Saambiga
@saambiga
Membre depuis il y a 5 mois
16 abonnés
4 suivis
161 quiz
Filtres
AvancéSciences
0.0
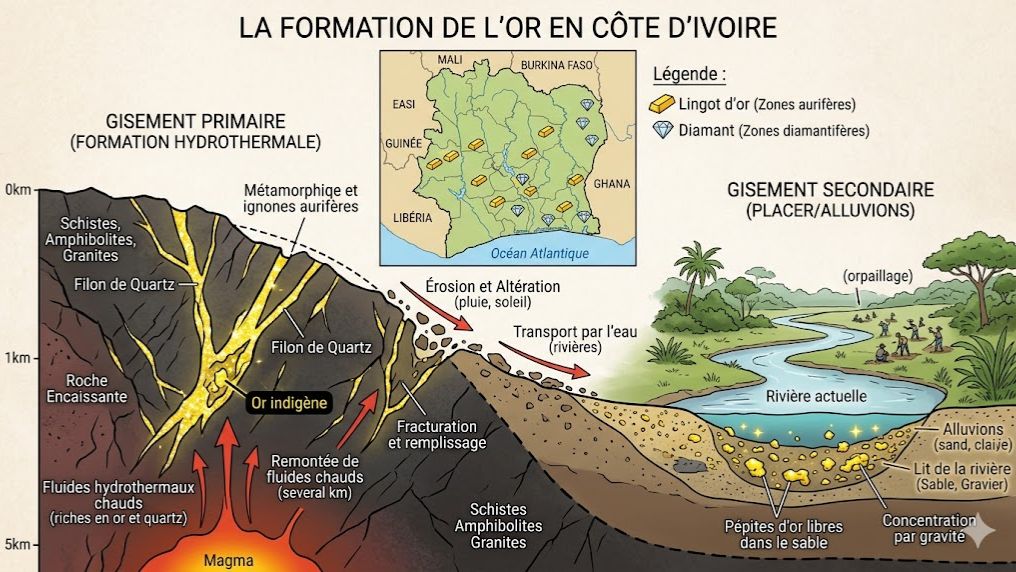
Ce quiz interactif de SVT est spécialement conçu pour les élèves des classes de Terminale D et C en Côte d'Ivoire, conformément au programme officiel du Ministère de l'Éducation Nationale. À travers 10 questions ciblées, révisez la Leçon 1 du Thème 1 sur les ressources minières. Plongez au cœur du sous-sol ivoirien pour découvrir la localisation des gisements stratégiques comme l'or d'Ity et de Tongon, le diamant de Séguéla, le manganèse de Lauzoua, ou encore le nickel de Biankouma.
Le test aborde des concepts géologiques fondamentaux tels que les formations birimiennes, les notions de roche encaissante et de minerai, ainsi que les mécanismes de formation des gisements primaires (processus hydrothermaux) et secondaires (placers alluvionnaires). Idéal pour préparer le BAC, ce quiz offre des explications détaillées pour chaque réponse, permettant de consolider ses connaissances sur les richesses naturelles du pays et les processus sédimentaires et magmatiques associés. Améliorez votre score, maîtrisez le lexique scientifique et réussissez vos évaluations avec Kwiizoo !
### 💡 Résumé du Cours (Aide-mémoire) ###
Contexte Géologique : La majeure partie des gisements ivoiriens se trouve dans le socle précambrien, particulièrement dans les zones de roches vertes appelées le Birimien.
Les Ressources Majeures :
- Or : Gisements d'Ity (Zouan-Hounien), Tongon (M'bengué), Bonikro (Hiré).
- Diamant : Tortiya et Séguéla.
- Manganèse : Lauzoua (Grand-Lahou).
- Bauxite (Aluminium) : Benene (Bongouanou).
- Nickel/Cobalt : Biankouma et Sipilou.
Mécanismes de Formation (Exemple de l'Or) :
1. Gisement Primaire : Formé en profondeur. Des fluides chauds (hydrothermaux) chargés de métaux circulent dans des fractures de la roche encaissante et déposent l'or dans des filons de quartz.
2. Gisement Secondaire (Placer) : Formé en surface. L'érosion dégrade les filons primaires ; l'or, très dense, est transporté par l'eau et s'accumule dans les alluvions (lits des rivières).
Définitions :
- Roche encaissante : Roche hôte entourant le gisement.
- Minerai : Roche contenant une substance utile en quantité suffisante pour une exploitation rentable.
Le test aborde des concepts géologiques fondamentaux tels que les formations birimiennes, les notions de roche encaissante et de minerai, ainsi que les mécanismes de formation des gisements primaires (processus hydrothermaux) et secondaires (placers alluvionnaires). Idéal pour préparer le BAC, ce quiz offre des explications détaillées pour chaque réponse, permettant de consolider ses connaissances sur les richesses naturelles du pays et les processus sédimentaires et magmatiques associés. Améliorez votre score, maîtrisez le lexique scientifique et réussissez vos évaluations avec Kwiizoo !
### 💡 Résumé du Cours (Aide-mémoire) ###
Contexte Géologique : La majeure partie des gisements ivoiriens se trouve dans le socle précambrien, particulièrement dans les zones de roches vertes appelées le Birimien.
Les Ressources Majeures :
- Or : Gisements d'Ity (Zouan-Hounien), Tongon (M'bengué), Bonikro (Hiré).
- Diamant : Tortiya et Séguéla.
- Manganèse : Lauzoua (Grand-Lahou).
- Bauxite (Aluminium) : Benene (Bongouanou).
- Nickel/Cobalt : Biankouma et Sipilou.
Mécanismes de Formation (Exemple de l'Or) :
1. Gisement Primaire : Formé en profondeur. Des fluides chauds (hydrothermaux) chargés de métaux circulent dans des fractures de la roche encaissante et déposent l'or dans des filons de quartz.
2. Gisement Secondaire (Placer) : Formé en surface. L'érosion dégrade les filons primaires ; l'or, très dense, est transporté par l'eau et s'accumule dans les alluvions (lits des rivières).
Définitions :
- Roche encaissante : Roche hôte entourant le gisement.
- Minerai : Roche contenant une substance utile en quantité suffisante pour une exploitation rentable.
0 essai(s) il y a 25 minute(s)
10
AvancéSciences
0.0
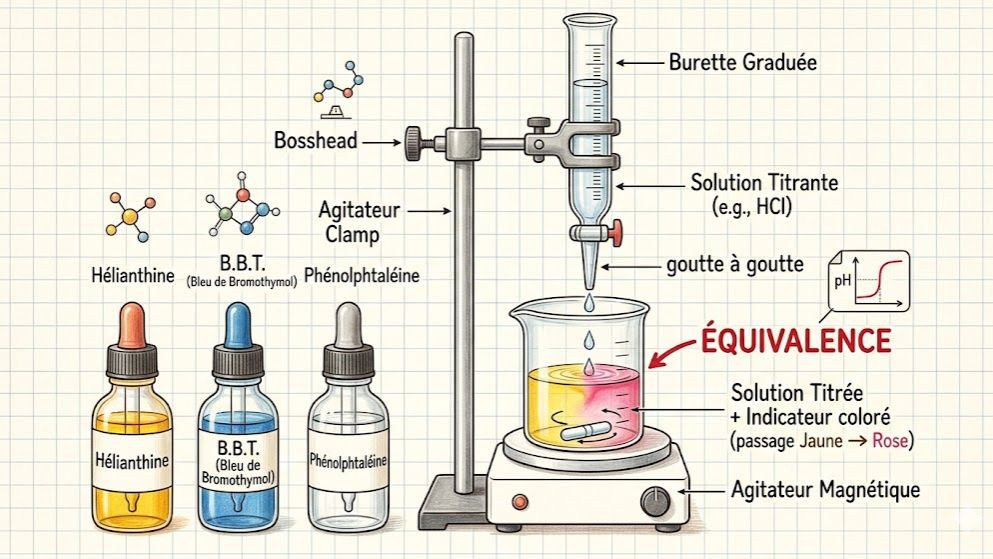
Maîtrisez les techniques de laboratoire avec ce quiz final sur le dosage acido-basique, conforme au programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez votre capacité à déterminer la concentration d'une solution commerciale, comme le vinaigre, à travers le dosage colorimétrique. Que vous soyez élève au Lycée des Jeunes Filles de Bouaké ou ailleurs, ce test vous permet de réviser le protocole expérimental, le choix judicieux de l'indicateur coloré (B.B.T, hélianthine, phénolphtaléine) et le calcul des concentrations molaires à l'équivalence. Apprenez à schématiser un dispositif de dosage et à interpréter le changement de couleur pour identifier le point final.
Évaluez vos compétences sur la relation $C_A \cdot V_A = C_B \cdot V_B$ et comprenez l'intérêt industriel et domestique de ces mesures de précision. Un outil de révision ultime pour valider vos acquis avant le Baccalauréat avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Principe du dosage : Déterminer la concentration inconnue d'une espèce en solution en la faisant réagir totalement avec une autre espèce de concentration connue (le réactif titrant).
Dispositif expérimental : Comprend une burette graduée (contenant le réactif titrant), un bécher (contenant la solution à doser) et un agitateur magnétique.
Équivalence acido-basique : Moment où les réactifs ont été introduits dans des proportions stœchiométriques ; il y a changement de nature du milieu (de l'acide vers le basique ou inversement).
Dosage colorimétrique : Utilise un indicateur coloré dont la zone de virage contient le pH à l'équivalence pour visualiser le point final.
Application : Dosage de l'acide éthanoïque du vinaigre par une solution de soude.
Évaluez vos compétences sur la relation $C_A \cdot V_A = C_B \cdot V_B$ et comprenez l'intérêt industriel et domestique de ces mesures de précision. Un outil de révision ultime pour valider vos acquis avant le Baccalauréat avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Principe du dosage : Déterminer la concentration inconnue d'une espèce en solution en la faisant réagir totalement avec une autre espèce de concentration connue (le réactif titrant).
Dispositif expérimental : Comprend une burette graduée (contenant le réactif titrant), un bécher (contenant la solution à doser) et un agitateur magnétique.
Équivalence acido-basique : Moment où les réactifs ont été introduits dans des proportions stœchiométriques ; il y a changement de nature du milieu (de l'acide vers le basique ou inversement).
Dosage colorimétrique : Utilise un indicateur coloré dont la zone de virage contient le pH à l'équivalence pour visualiser le point final.
Application : Dosage de l'acide éthanoïque du vinaigre par une solution de soude.
1 essai(s) il y a 3 heure(s)
10
AvancéSciences
0.0
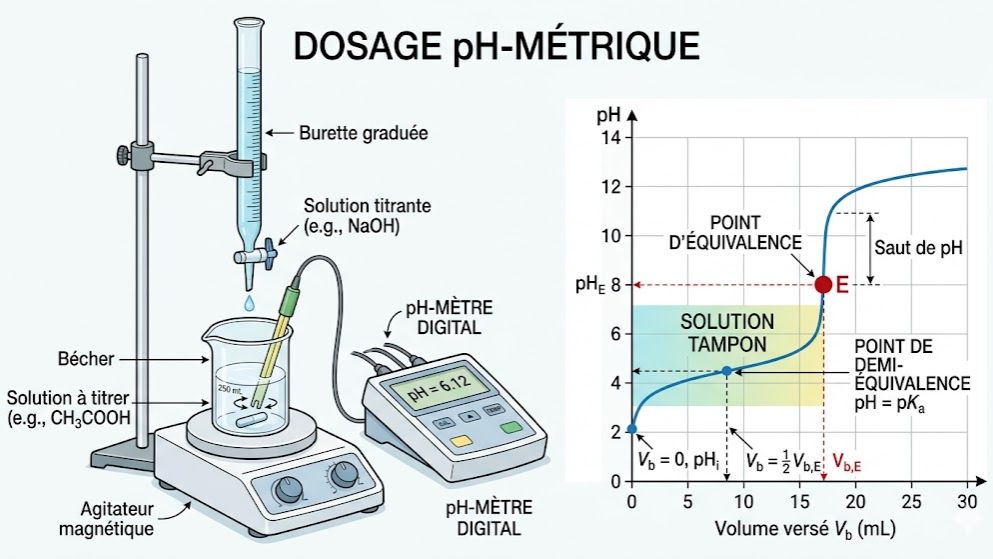
Maîtrisez les dosages et les solutions tampons avec ce quiz complet conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre compréhension des réactions entre acides et bases (forts et faibles), le tracé et l'exploitation des courbes pH-métriques, ainsi que la définition de l'équivalence.
Que vous soyez élève au Lycée Moderne d’Agboville ou ailleurs, révisez les caractéristiques essentielles des solutions tampons : leur préparation, leurs propriétés de résistance aux variations de pH et leur intérêt biologique ou agronomique. Apprenez à déterminer la demi-équivalence et la relation pH = pKa. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre comment stabiliser le pH dans des systèmes complexes avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
Réactions acido-basiques : Ce sont des transferts de protons $H^+$ entre un acide et une base. Elles sont généralement exothermiques et totales lorsqu'au moins l'un des réactifs est fort.
Dosage pH-métrique : Permet de déterminer la concentration d'une solution.
- Équivalence : Point où les réactifs ont été mélangés dans des proportions stoechiométriques.
- Demi-équivalence : Pour un dosage acide faible/base forte, à ce point, $pH = pK_A$.
Solution Tampon : Solution dont le pH varie très peu lors de l'ajout modéré d'un acide, d'une base ou lors d'une dilution.
- Préparation : Mélange équimolaire d'un acide faible et de sa base conjuguée, ou par demi-équivalence d'un dosage.
Que vous soyez élève au Lycée Moderne d’Agboville ou ailleurs, révisez les caractéristiques essentielles des solutions tampons : leur préparation, leurs propriétés de résistance aux variations de pH et leur intérêt biologique ou agronomique. Apprenez à déterminer la demi-équivalence et la relation pH = pKa. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre comment stabiliser le pH dans des systèmes complexes avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
Réactions acido-basiques : Ce sont des transferts de protons $H^+$ entre un acide et une base. Elles sont généralement exothermiques et totales lorsqu'au moins l'un des réactifs est fort.
Dosage pH-métrique : Permet de déterminer la concentration d'une solution.
- Équivalence : Point où les réactifs ont été mélangés dans des proportions stoechiométriques.
- Demi-équivalence : Pour un dosage acide faible/base forte, à ce point, $pH = pK_A$.
Solution Tampon : Solution dont le pH varie très peu lors de l'ajout modéré d'un acide, d'une base ou lors d'une dilution.
- Préparation : Mélange équimolaire d'un acide faible et de sa base conjuguée, ou par demi-équivalence d'un dosage.
1 essai(s) il y a 4 heure(s)
10
AvancéSciences
0.0
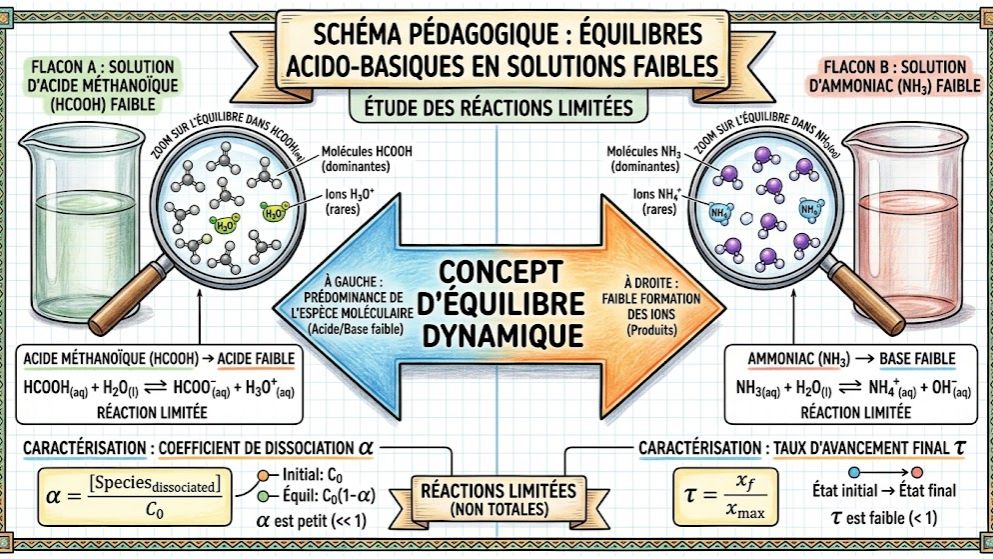
Maîtrisez les concepts d'équilibre chimique avec ce quiz sur les acides et bases faibles, conforme au programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez votre compréhension sur la réaction partielle de l'acide éthanoïque ou de l'ammoniac avec l'eau.
Que vous soyez élève au Lycée Moderne de Bangolo ou ailleurs, ce test vous permet de réviser des notions clés comme le coefficient d'ionisation ($\alpha$), l'équilibre chimique et l'effet de la dilution sur l'ionisation des espèces. Évaluez votre capacité à calculer les concentrations molaires des espèces chimiques présentes dans une solution faible et à interpréter les différences de pH entre solutions de même concentration. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien et maîtriser la chimie générale avec Kwiizoo.
1. Définitions Fondamentales
. Acide Faible : Espèce chimique dont la réaction avec l’eau est partielle (ou limitée).
Équation : $AH + H_2O \rightleftharpoons A^- + H_3O^+$
Exemple : L’acide éthanoïque ($CH_3COOH$).
. Base Faible : Espèce dont la réaction avec l’eau est incomplète.
Équation : $B + H_2O \rightleftharpoons BH^+ + OH^-$
Exemple : L’ammoniac ($NH_3$).
2. Le Coefficient d'Ionisation ($\alpha$)
C'est un élément clé de la page 29 du programme ivoirien.
. Formule : $\alpha = \frac{\text{quantité d'acide réagi}}{\text{quantité d'acide initial}}$
. Propriété : Pour un acide faible, $0 < \alpha < 1$. Plus la solution est diluée, plus $\alpha$ augmente (loi de dilution d'Ostwald).
3. Étude Quantitative et pH
. Pour un acide faible : Le pH est supérieur à celui d'un acide fort de même concentration ($pH > -\log C$).
. Pour une base faible : Le pH est inférieur à celui d'une base forte de même concentration.
4. La Constante d'Acidité ($K_A$ et $pK_A$)
La force d'un couple est caractérisée par sa constante à l'équilibre :
$K_A = \frac{[A^-]_{éq} \cdot [H_3O^+]_{éq}}{[AH]_{éq}}$
$pK_A = -\log K_A$
. Règle de classification : Un acide est d'autant plus fort que son $K_A$ est grand ou que son $pK_A$ est petit.
Que vous soyez élève au Lycée Moderne de Bangolo ou ailleurs, ce test vous permet de réviser des notions clés comme le coefficient d'ionisation ($\alpha$), l'équilibre chimique et l'effet de la dilution sur l'ionisation des espèces. Évaluez votre capacité à calculer les concentrations molaires des espèces chimiques présentes dans une solution faible et à interpréter les différences de pH entre solutions de même concentration. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien et maîtriser la chimie générale avec Kwiizoo.
1. Définitions Fondamentales
. Acide Faible : Espèce chimique dont la réaction avec l’eau est partielle (ou limitée).
Équation : $AH + H_2O \rightleftharpoons A^- + H_3O^+$
Exemple : L’acide éthanoïque ($CH_3COOH$).
. Base Faible : Espèce dont la réaction avec l’eau est incomplète.
Équation : $B + H_2O \rightleftharpoons BH^+ + OH^-$
Exemple : L’ammoniac ($NH_3$).
2. Le Coefficient d'Ionisation ($\alpha$)
C'est un élément clé de la page 29 du programme ivoirien.
. Formule : $\alpha = \frac{\text{quantité d'acide réagi}}{\text{quantité d'acide initial}}$
. Propriété : Pour un acide faible, $0 < \alpha < 1$. Plus la solution est diluée, plus $\alpha$ augmente (loi de dilution d'Ostwald).
3. Étude Quantitative et pH
. Pour un acide faible : Le pH est supérieur à celui d'un acide fort de même concentration ($pH > -\log C$).
. Pour une base faible : Le pH est inférieur à celui d'une base forte de même concentration.
4. La Constante d'Acidité ($K_A$ et $pK_A$)
La force d'un couple est caractérisée par sa constante à l'équilibre :
$K_A = \frac{[A^-]_{éq} \cdot [H_3O^+]_{éq}}{[AH]_{éq}}$
$pK_A = -\log K_A$
. Règle de classification : Un acide est d'autant plus fort que son $K_A$ est grand ou que son $pK_A$ est petit.
1 essai(s) il y a 22 heure(s)
10
AvancéSciences
0.0
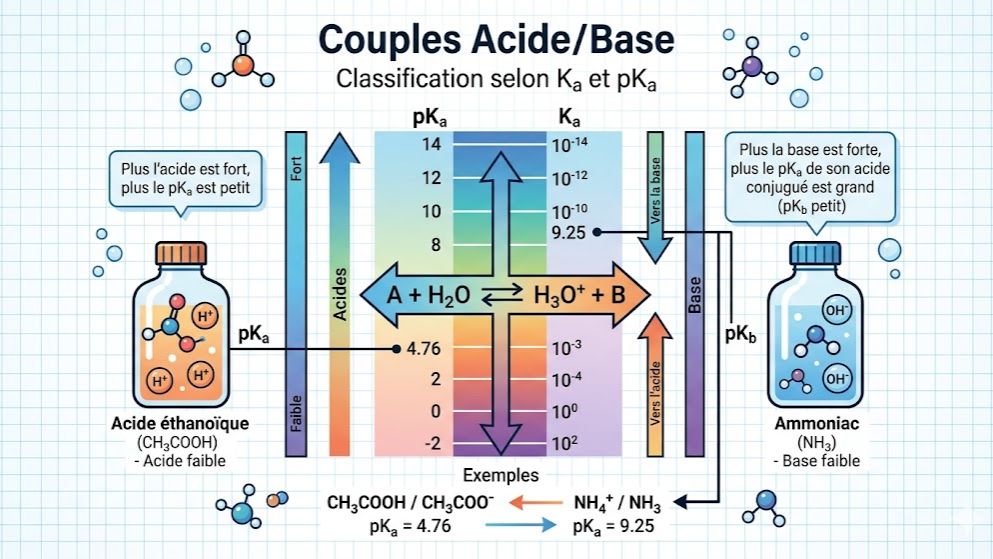
Maîtrisez la force relative des acides et des bases avec ce quiz sur les couples acido-basiques, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre compréhension des définitions de Brönsted et votre capacité à identifier les acides et leurs bases conjuguées.
Que vous soyez élève au Lycée Moderne d’Agnibilékrou ou ailleurs, ce quiz vous permet de réviser les constantes d'acidité $K_A$ et le $pK_A$, outils indispensables pour classer les couples selon leur force. Apprenez à déterminer les domaines de prédominance et à choisir le bon indicateur coloré grâce à sa zone de virage. Évaluez vos compétences sur la relation $pH = pK_A + \log([B]/[A])$ et comprenez pourquoi certains acides sont plus forts que d'autres. Un entraînement idéal pour réussir le Baccalauréat ivoirien et exceller en chimie générale avec Kwiizoo.
## Résumé du Cours (Aide-mémoire). ##
Définition de Brönsted : Un acide est une espèce capable de céder un proton $H^+$ ; une base est une espèce capable d'en capter un.
Couple Acide/Base : Formé par deux espèces qui se transforment l'une en l'autre par gain ou perte d'un proton.
Constante d'acidité ($K_A$) : Grandeur caractérisant la force d'un acide dans l'eau. Plus le $K_A$ est grand (ou le $pK_A$ petit), plus l'acide est fort.
Relation fondamentale : $pH = pK_A + \log \frac{[\text{Base}]}{[\text{Acide}]}$.
Domaine de prédominance :
- Si $pH < pK_A$ : l'Acide prédomine.
- Si $pH > pK_A$ : la Base prédomine.
Que vous soyez élève au Lycée Moderne d’Agnibilékrou ou ailleurs, ce quiz vous permet de réviser les constantes d'acidité $K_A$ et le $pK_A$, outils indispensables pour classer les couples selon leur force. Apprenez à déterminer les domaines de prédominance et à choisir le bon indicateur coloré grâce à sa zone de virage. Évaluez vos compétences sur la relation $pH = pK_A + \log([B]/[A])$ et comprenez pourquoi certains acides sont plus forts que d'autres. Un entraînement idéal pour réussir le Baccalauréat ivoirien et exceller en chimie générale avec Kwiizoo.
## Résumé du Cours (Aide-mémoire). ##
Définition de Brönsted : Un acide est une espèce capable de céder un proton $H^+$ ; une base est une espèce capable d'en capter un.
Couple Acide/Base : Formé par deux espèces qui se transforment l'une en l'autre par gain ou perte d'un proton.
Constante d'acidité ($K_A$) : Grandeur caractérisant la force d'un acide dans l'eau. Plus le $K_A$ est grand (ou le $pK_A$ petit), plus l'acide est fort.
Relation fondamentale : $pH = pK_A + \log \frac{[\text{Base}]}{[\text{Acide}]}$.
Domaine de prédominance :
- Si $pH < pK_A$ : l'Acide prédomine.
- Si $pH > pK_A$ : la Base prédomine.
1 essai(s) il y a 23 heure(s)
10
AvancéSciences
0.0
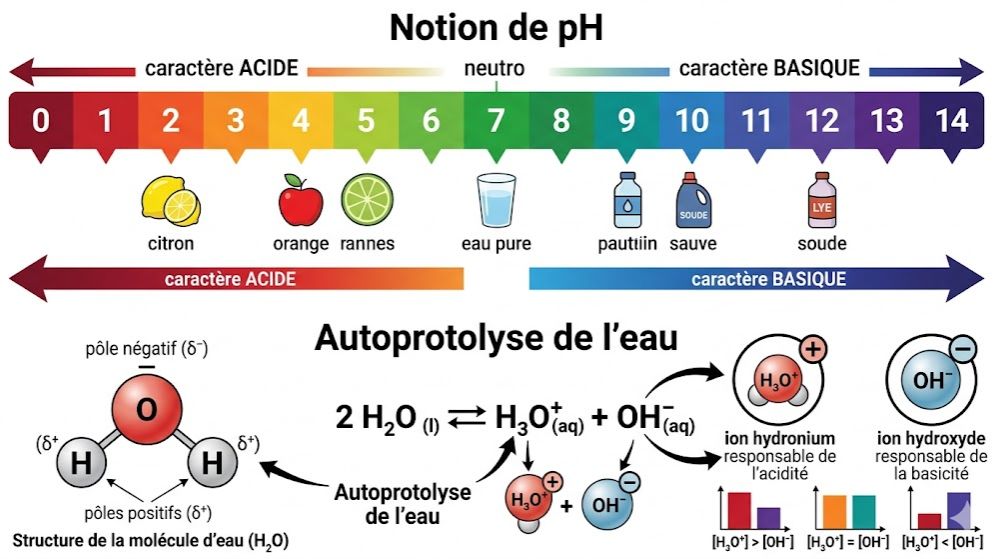
Maîtrisez les fondamentaux de la chimie des solutions avec ce quiz sur les solutions aqueuses et la notion de pH, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez vos connaissances sur les propriétés uniques de l'eau en tant que solvant dipolaire, ionisant et hydratant.
Que vous étudiiez au Lycée Moderne d’Azaguié ou ailleurs, ce test vous permet de réviser l'équation d'autoprotolyse de l'eau , le produit ionique $K_e$ et la définition logarithmique du pH. Évaluez votre capacité à vérifier l'électroneutralité d'une solution et à calculer les concentrations molaires des espèces chimiques présentes. Apprenez à classer les solutions en fonction de leur acidité ou basicité et comprenez les limites de validité de la relation pH = -log[H3O+]. Un outil de révision essentiel pour réussir le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
L'Eau, un solvant particulier : Molécule polaire capable de disloquer, d'ioniser et d'hydrater les solutés.
Autoprotolyse de l'eau : Réaction entre deux molécules d'eau produisant des ions hydronium et hydroxyde : $2H_2O \rightleftharpoons H_3O^+ + OH^-$.
Produit ionique ($K_e$) : À 25°C, $K_e = [H_3O^+][OH^-] = 10^{-14}$.
Définition du pH : $pH = -\log[H_3O^+]$. Cette relation est valable pour des solutions diluées ($C \le 0,1 \text{ mol/L}$).
Lois de conservation :
- Électroneutralité : La somme des charges positives est égale à la somme des charges négatives.
- Conservation de la matière : La quantité de matière de l'élément chimique se conserve lors de la dissolution.
Que vous étudiiez au Lycée Moderne d’Azaguié ou ailleurs, ce test vous permet de réviser l'équation d'autoprotolyse de l'eau , le produit ionique $K_e$ et la définition logarithmique du pH. Évaluez votre capacité à vérifier l'électroneutralité d'une solution et à calculer les concentrations molaires des espèces chimiques présentes. Apprenez à classer les solutions en fonction de leur acidité ou basicité et comprenez les limites de validité de la relation pH = -log[H3O+]. Un outil de révision essentiel pour réussir le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
L'Eau, un solvant particulier : Molécule polaire capable de disloquer, d'ioniser et d'hydrater les solutés.
Autoprotolyse de l'eau : Réaction entre deux molécules d'eau produisant des ions hydronium et hydroxyde : $2H_2O \rightleftharpoons H_3O^+ + OH^-$.
Produit ionique ($K_e$) : À 25°C, $K_e = [H_3O^+][OH^-] = 10^{-14}$.
Définition du pH : $pH = -\log[H_3O^+]$. Cette relation est valable pour des solutions diluées ($C \le 0,1 \text{ mol/L}$).
Lois de conservation :
- Électroneutralité : La somme des charges positives est égale à la somme des charges négatives.
- Conservation de la matière : La quantité de matière de l'élément chimique se conserve lors de la dissolution.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
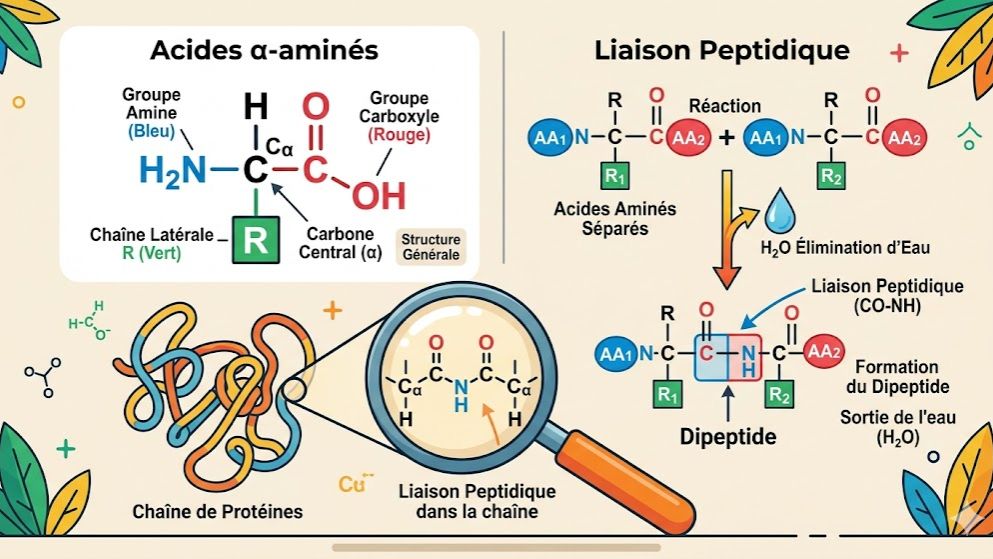
Plongez dans la chimie du vivant avec ce quiz sur les acides $\alpha$-aminés, conçu selon le programme de Physique-Chimie de la Terminale D en Côte d'Ivoire. Ce test interactif vous permet de réviser la structure bifonctionnelle de ces molécules essentielles, portant à la fois un groupe amino et un groupe carboxyle sur le même carbone.
Que vous soyez élève dans un lycée ivoirien ou passionné de biochimie, testez vos connaissances sur la nomenclature IUPAC, le caractère amphotère du zwitterion (ion dipolaire) et la formation de la liaison peptidique. Apprenez à identifier les dipeptides et les protéines, et révisez les tests caractéristiques comme la réaction du Biuret. Un outil de révision stratégique pour maîtriser ce chapitre clé du Baccalauréat ivoirien et comprendre comment notre corps construit ses propres protéines avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Définition : Un acide $\alpha$-aminé possède un groupe amine ($-NH_2$) et un groupe carboxyle ($-COOH$) fixés sur le même atome de carbone dit "carbone $\alpha$".
Structure et pH : En solution aqueuse, ils existent sous forme d'ion dipolaire appelé zwitterion ou amphion.
Propriétés amphotères : Le zwitterion se comporte comme une base en milieu acide et comme un acide en milieu basique.
Liaison Peptidique : C'est une liaison amide ($-NH-CO-$) qui se forme par élimination d'une molécule d'eau entre deux acides $\alpha$-aminés.
Protéines : Ce sont des macromolécules formées par l'enchaînement d'un grand nombre d'acides aminés (généralement plus de 50).
Identification : La réaction de Biuret permet de mettre en évidence la présence de liaisons peptidiques (coloration violette en présence d'ions $Cu^{2+}$ en milieu basique).
Que vous soyez élève dans un lycée ivoirien ou passionné de biochimie, testez vos connaissances sur la nomenclature IUPAC, le caractère amphotère du zwitterion (ion dipolaire) et la formation de la liaison peptidique. Apprenez à identifier les dipeptides et les protéines, et révisez les tests caractéristiques comme la réaction du Biuret. Un outil de révision stratégique pour maîtriser ce chapitre clé du Baccalauréat ivoirien et comprendre comment notre corps construit ses propres protéines avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Définition : Un acide $\alpha$-aminé possède un groupe amine ($-NH_2$) et un groupe carboxyle ($-COOH$) fixés sur le même atome de carbone dit "carbone $\alpha$".
Structure et pH : En solution aqueuse, ils existent sous forme d'ion dipolaire appelé zwitterion ou amphion.
Propriétés amphotères : Le zwitterion se comporte comme une base en milieu acide et comme un acide en milieu basique.
Liaison Peptidique : C'est une liaison amide ($-NH-CO-$) qui se forme par élimination d'une molécule d'eau entre deux acides $\alpha$-aminés.
Protéines : Ce sont des macromolécules formées par l'enchaînement d'un grand nombre d'acides aminés (généralement plus de 50).
Identification : La réaction de Biuret permet de mettre en évidence la présence de liaisons peptidiques (coloration violette en présence d'ions $Cu^{2+}$ en milieu basique).
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
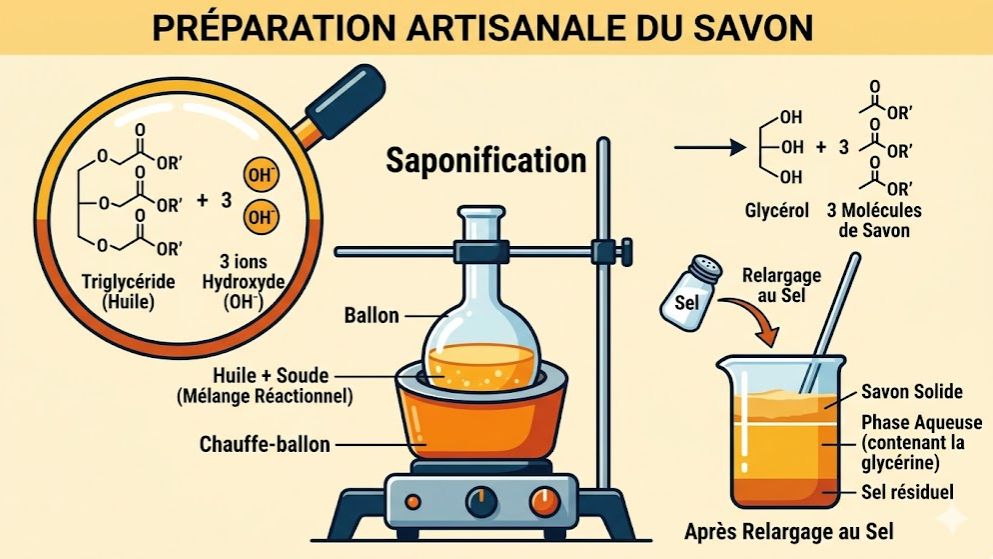
Devenez incollable sur la fabrication du savon avec ce quiz pédagogique basé sur le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. À travers ce test, révisez la réaction de saponification, un processus chimique fondamental où un corps gras (triester) réagit avec une base forte pour produire du savon et du glycérol.
Que vous soyez élève au Lycée Municipal de Williamsville ou ailleurs, ce quiz évalue votre connaissance des caractéristiques de cette réaction : elle est lente à froid, mais totale et exothermique. Apprenez à identifier la formule générale d'un savon, ses propriétés détergentes et les étapes de fabrication comme le relargage. Un outil indispensable pour maîtriser la chimie organique et réussir votre Baccalauréat avec Kwiizoo, l'application leader pour l'excellence académique ivoirienne.
## Résumé du Cours (Aide-mémoire) ##
# Définition : La saponification est l'hydrolyse en milieu basique (soude ou potasse) d'un ester, plus précisément d'un corps gras (triglycéride).
# Réaction : Corps gras + Base forte (NaOH ou KOH) $\rightarrow$ Savon + Glycérol.
# Caractéristiques : C'est une réaction lente (à température ambiante), mais totale et exothermique.
# Structure d'un savon : Un savon est un mélange de carboxylates de sodium (savon dur) ou de potassium (savon mou). Il possède une tête hydrophile (qui aime l'eau) et une queue hydrophobe/lipophile (qui aime les graisses).
# Le Relargage : Étape consistant à ajouter du sel (NaCl) pour précipiter le savon et le séparer du mélange.
Que vous soyez élève au Lycée Municipal de Williamsville ou ailleurs, ce quiz évalue votre connaissance des caractéristiques de cette réaction : elle est lente à froid, mais totale et exothermique. Apprenez à identifier la formule générale d'un savon, ses propriétés détergentes et les étapes de fabrication comme le relargage. Un outil indispensable pour maîtriser la chimie organique et réussir votre Baccalauréat avec Kwiizoo, l'application leader pour l'excellence académique ivoirienne.
## Résumé du Cours (Aide-mémoire) ##
# Définition : La saponification est l'hydrolyse en milieu basique (soude ou potasse) d'un ester, plus précisément d'un corps gras (triglycéride).
# Réaction : Corps gras + Base forte (NaOH ou KOH) $\rightarrow$ Savon + Glycérol.
# Caractéristiques : C'est une réaction lente (à température ambiante), mais totale et exothermique.
# Structure d'un savon : Un savon est un mélange de carboxylates de sodium (savon dur) ou de potassium (savon mou). Il possède une tête hydrophile (qui aime l'eau) et une queue hydrophobe/lipophile (qui aime les graisses).
# Le Relargage : Étape consistant à ajouter du sel (NaCl) pour précipiter le savon et le séparer du mélange.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
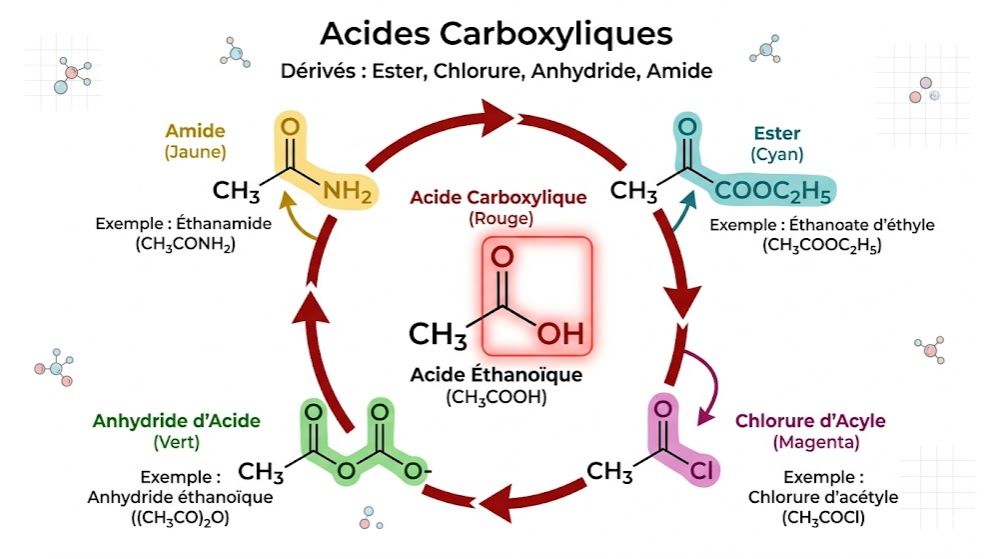
Maîtrisez la réactivité des fonctions oxygénées avec ce quiz complet sur les acides carboxyliques et leurs dérivés, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre connaissance du groupe fonctionnel carboxyle et des familles dérivées comme les esters, les chlorures d'acyle, les anhydrides d'acide et les amides. Que vous soyez élève au Lycée Moderne HKB 1 de Daoukro ou ailleurs, révisez la nomenclature IUPAC, les propriétés acides et les méthodes de synthèse par estérification ou hydrolyse.
Apprenez à écrire les équations-bilans de passage entre ces différentes molécules indispensables dans l'industrie des médicaments et des plastiques. Un outil pédagogique performant pour préparer votre Baccalauréat et exceller en chimie organique avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
. Groupe Carboxyle : Le groupe fonctionnel est -COOH. Sa formule générale est $R-COOH$ ou $C_nH_{2n}O_2$.
. Les Dérivés : Ils sont obtenus par remplacement du groupement -OH de l'acide:
- Chlorure d'acyle : $R-COCl$.
- Anhydride d'acide : $R-CO-O-CO-R$.
- Ester : $R-COOR'$.
- Amide : $R-CONH_2$.
. Propriétés : Les acides carboxyliques sont des acides faibles dans l'eau.
. Réactions clés :
- Estérification : Acide + Alcool $\rightleftharpoons$ Ester + Eau (réaction lente et réversible).
- Obtention d'un ester avec dérivé : Chlorure d'acyle (ou anhydride) + Alcool $\rightarrow$ Ester + $HCl$ (réaction rapide et totale).
Apprenez à écrire les équations-bilans de passage entre ces différentes molécules indispensables dans l'industrie des médicaments et des plastiques. Un outil pédagogique performant pour préparer votre Baccalauréat et exceller en chimie organique avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
. Groupe Carboxyle : Le groupe fonctionnel est -COOH. Sa formule générale est $R-COOH$ ou $C_nH_{2n}O_2$.
. Les Dérivés : Ils sont obtenus par remplacement du groupement -OH de l'acide:
- Chlorure d'acyle : $R-COCl$.
- Anhydride d'acide : $R-CO-O-CO-R$.
- Ester : $R-COOR'$.
- Amide : $R-CONH_2$.
. Propriétés : Les acides carboxyliques sont des acides faibles dans l'eau.
. Réactions clés :
- Estérification : Acide + Alcool $\rightleftharpoons$ Ester + Eau (réaction lente et réversible).
- Obtention d'un ester avec dérivé : Chlorure d'acyle (ou anhydride) + Alcool $\rightarrow$ Ester + $HCl$ (réaction rapide et totale).
0 essai(s) il y a 2 jour(s)
10
AvancéSciences
0.0
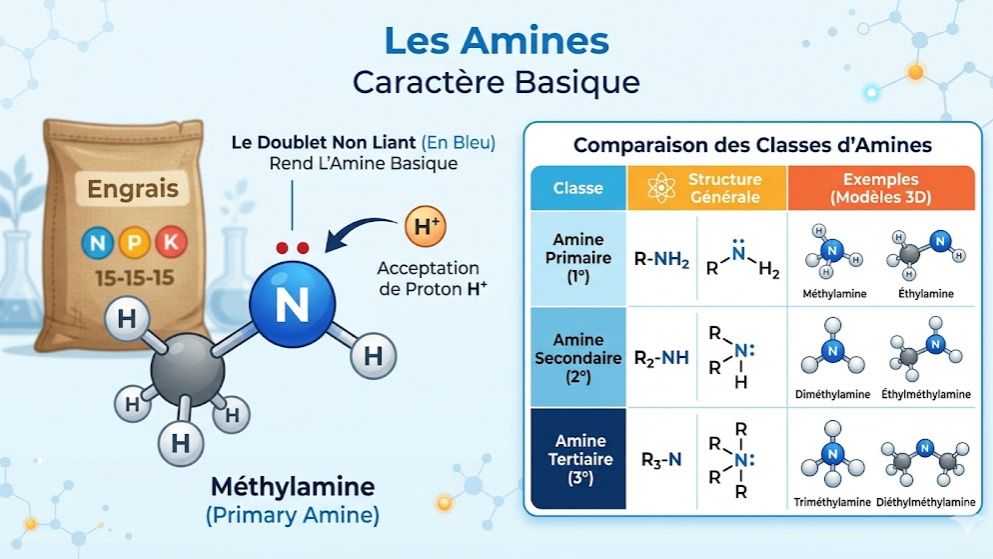
Maîtrisez la chimie des composés azotés avec ce quiz complet sur les amines, conçu pour le programme de Physique-Chimie de la Terminale D en Côte d'Ivoire. Que vous soyez élève au Lycée Moderne de Dimbokro ou ailleurs, ce test vous permet de réviser la structure électronique de l'azote et la formule générale des amines $C_nH_{2n+1}NH_2$ pour les monoamines saturées.
Évaluez vos connaissances sur la classification des amines en trois classes (primaire, secondaire, tertiaire) et maîtrisez les règles de nomenclature IUPAC. Ce quiz aborde également les propriétés chimiques fondamentales : le caractère basique dû au doublet non liant de l'azote et le caractère nucléophile. Préparez efficacement votre Baccalauréat avec Kwiizoo et comprenez l'importance des amines dans la fabrication des engrais NPK et du vivant.
## Résumé du Cours (Aide-mémoire) ##
. Définition : Les amines sont des dérivés de l'ammoniac ($NH_3$) où un ou plusieurs atomes d'hydrogène sont remplacés par des groupes carbonés.
. Les Trois Classes:
- Primaire : L'azote est lié à 1 groupe alkyl ($R-NH_2$).
- Secondaire : L'azote est lié à 2 groupes alkyls ($R-NH-R'$).
- Tertiaire : L'azote est lié à 3 groupes alkyls ($R-N(R')-R''$).
. Propriétés Physiques : La structure électronique de l'azote confère aux amines des propriétés particulières.
. Propriétés Chimiques :
- Caractère basique : Les amines acceptent un proton $H^+$ grâce au doublet non liant de l'azote.
- Caractère nucléophile : Elles peuvent attaquer des centres pauvres en électrons.
. Importance : Elles sont liées à l'azote du trio "NPK" des engrais essentiels en agriculture.
Évaluez vos connaissances sur la classification des amines en trois classes (primaire, secondaire, tertiaire) et maîtrisez les règles de nomenclature IUPAC. Ce quiz aborde également les propriétés chimiques fondamentales : le caractère basique dû au doublet non liant de l'azote et le caractère nucléophile. Préparez efficacement votre Baccalauréat avec Kwiizoo et comprenez l'importance des amines dans la fabrication des engrais NPK et du vivant.
## Résumé du Cours (Aide-mémoire) ##
. Définition : Les amines sont des dérivés de l'ammoniac ($NH_3$) où un ou plusieurs atomes d'hydrogène sont remplacés par des groupes carbonés.
. Les Trois Classes:
- Primaire : L'azote est lié à 1 groupe alkyl ($R-NH_2$).
- Secondaire : L'azote est lié à 2 groupes alkyls ($R-NH-R'$).
- Tertiaire : L'azote est lié à 3 groupes alkyls ($R-N(R')-R''$).
. Propriétés Physiques : La structure électronique de l'azote confère aux amines des propriétés particulières.
. Propriétés Chimiques :
- Caractère basique : Les amines acceptent un proton $H^+$ grâce au doublet non liant de l'azote.
- Caractère nucléophile : Elles peuvent attaquer des centres pauvres en électrons.
. Importance : Elles sont liées à l'azote du trio "NPK" des engrais essentiels en agriculture.
0 essai(s) il y a 3 jour(s)
10
AvancéSciences
0.0
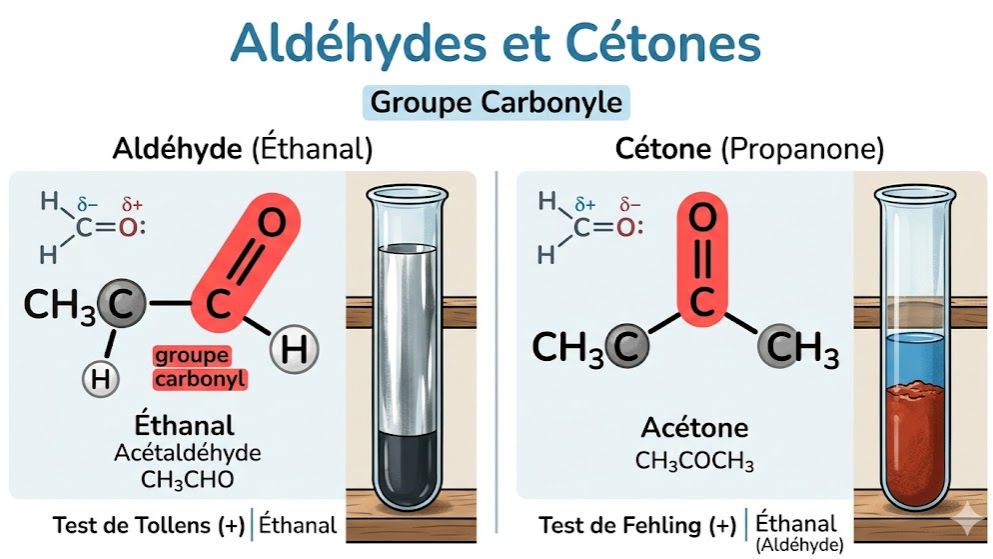
Maîtrisez la chimie des composés carbonylés avec ce quiz spécialisé sur les aldéhydes et les cétones, élaboré selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test interactif vous permet de réviser les notions fondamentales du groupe carbonyle ($C=O$), les formules générales et les règles de nomenclature IUPAC.
Que vous soyez au Lycée Moderne de M'Bahiakro ou ailleurs, apprenez à différencier ces deux familles grâce aux tests d'identification classiques : la 2,4-DNPH, le réactif de Schiff, la liqueur de Fehling et le réactif de Tollens (miroir d'argent). Évaluez vos compétences sur l'écriture des formules semi-développées et la compréhension du caractère réducteur spécifique aux aldéhydes. Un outil de révision complet pour réussir vos contrôles et le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
. Groupe Carbonyle : Le groupe fonctionnel commun est $>C=O$.
. Aldéhyde : Le carbone fonctionnel est en bout de chaîne et lié à au moins un hydrogène. Formule générale : $R-CHO$.
. Cétone : Le carbone fonctionnel est lié à deux autres atomes de carbone. Formule générale : $R-CO-R'$.
. Tests d'identification :
- Commun : La 2,4-DNPH donne un précipité jaune-orangé avec les deux familles.
- Spécifiques aux aldéhydes : Le réactif de Schiff (devient rose/violet), la liqueur de Fehling (précipité rouge brique) et le réactif de Tollens (dépôt d'argent métallique).
. Réduction : Seuls les aldéhydes ont un caractère réducteur marqué face aux oxydants doux.
Que vous soyez au Lycée Moderne de M'Bahiakro ou ailleurs, apprenez à différencier ces deux familles grâce aux tests d'identification classiques : la 2,4-DNPH, le réactif de Schiff, la liqueur de Fehling et le réactif de Tollens (miroir d'argent). Évaluez vos compétences sur l'écriture des formules semi-développées et la compréhension du caractère réducteur spécifique aux aldéhydes. Un outil de révision complet pour réussir vos contrôles et le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
. Groupe Carbonyle : Le groupe fonctionnel commun est $>C=O$.
. Aldéhyde : Le carbone fonctionnel est en bout de chaîne et lié à au moins un hydrogène. Formule générale : $R-CHO$.
. Cétone : Le carbone fonctionnel est lié à deux autres atomes de carbone. Formule générale : $R-CO-R'$.
. Tests d'identification :
- Commun : La 2,4-DNPH donne un précipité jaune-orangé avec les deux familles.
- Spécifiques aux aldéhydes : Le réactif de Schiff (devient rose/violet), la liqueur de Fehling (précipité rouge brique) et le réactif de Tollens (dépôt d'argent métallique).
. Réduction : Seuls les aldéhydes ont un caractère réducteur marqué face aux oxydants doux.
0 essai(s) il y a 3 jour(s)
10
AvancéSciences
0.0
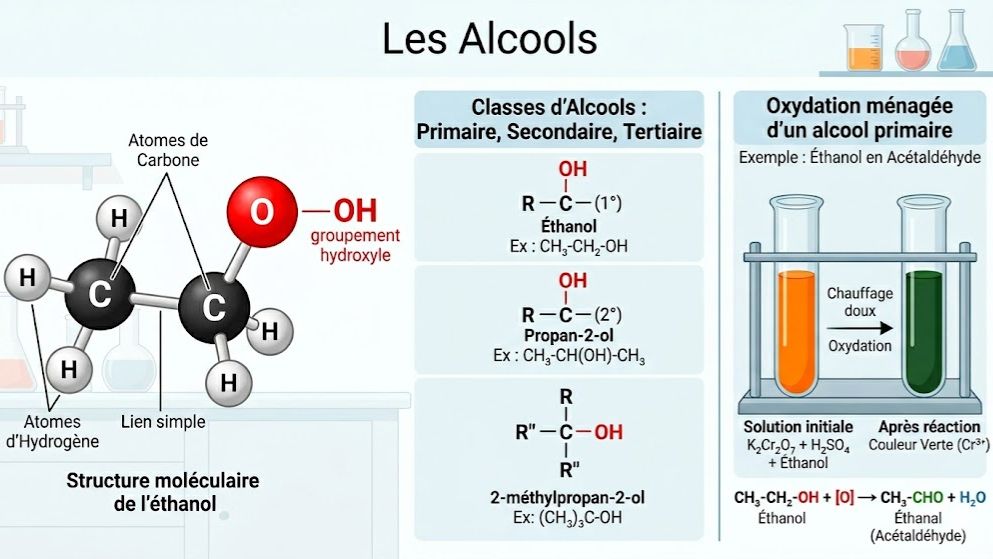
Maîtrisez la chimie des alcools avec ce quiz exhaustif conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Que vous étudiiez au Lycée Moderne de Treichville ou ailleurs, ce test vous permet de réviser les bases essentielles : définition d'un alcool, groupe fonctionnel hydroxyle et formule générale $C_nH_{2n+1}OH$. Testez votre capacité à identifier et nommer les trois classes d'alcools (primaire, secondaire, tertiaire) et à écrire les équations-bilans de réactions clés comme l'oxydation ménagée, la déshydratation et la combustion. Apprenez les méthodes de préparation industrielle par fermentation ou hydratation des alcènes.
Ce quiz aborde également les polyols comme le glycol et le glycérol. Préparez efficacement votre Baccalauréat et devenez un expert des composés organiques avec Kwiizoo, l'application de référence pour les lycéens ivoiriens.
## Résumé du Cours (Aide-mémoire) ##
* Définition : Un alcool est un composé organique où un groupe hydroxyle -OH est lié à un atome de carbone saturé.
* Classes d'alcools:
- Primaire : Le carbone fonctionnel est lié à 1 seul autre carbone.
- Secondaire : Le carbone fonctionnel est lié à 2 autres carbones.
- Tertiaire : Le carbone fonctionnel est lié à 3 autres carbones.
* Réactions chimiques :
- Oxydation ménagée : Un alcool primaire donne un aldéhyde puis un acide carboxylique ; un secondaire donne une cétone ; un tertiaire ne s'oxyde pas.
- Déshydratation : Intramoléculaire (donne un alcène) ou intermoléculaire (donne un éther-oxyde).
- Combustion : Produit du $CO_2$ et de l'eau avec dégagement de chaleur.
Ce quiz aborde également les polyols comme le glycol et le glycérol. Préparez efficacement votre Baccalauréat et devenez un expert des composés organiques avec Kwiizoo, l'application de référence pour les lycéens ivoiriens.
## Résumé du Cours (Aide-mémoire) ##
* Définition : Un alcool est un composé organique où un groupe hydroxyle -OH est lié à un atome de carbone saturé.
* Classes d'alcools:
- Primaire : Le carbone fonctionnel est lié à 1 seul autre carbone.
- Secondaire : Le carbone fonctionnel est lié à 2 autres carbones.
- Tertiaire : Le carbone fonctionnel est lié à 3 autres carbones.
* Réactions chimiques :
- Oxydation ménagée : Un alcool primaire donne un aldéhyde puis un acide carboxylique ; un secondaire donne une cétone ; un tertiaire ne s'oxyde pas.
- Déshydratation : Intramoléculaire (donne un alcène) ou intermoléculaire (donne un éther-oxyde).
- Combustion : Produit du $CO_2$ et de l'eau avec dégagement de chaleur.
0 essai(s) il y a 3 jour(s)
10