Physique-Chimie (3ème): Travail et Puissance Mécaniques , L'Essentiel sur l'Énergie et la Performance
IntermédiaireSciences
2 essai
0.0(0)
2 essai•il y a 27 jour(s)
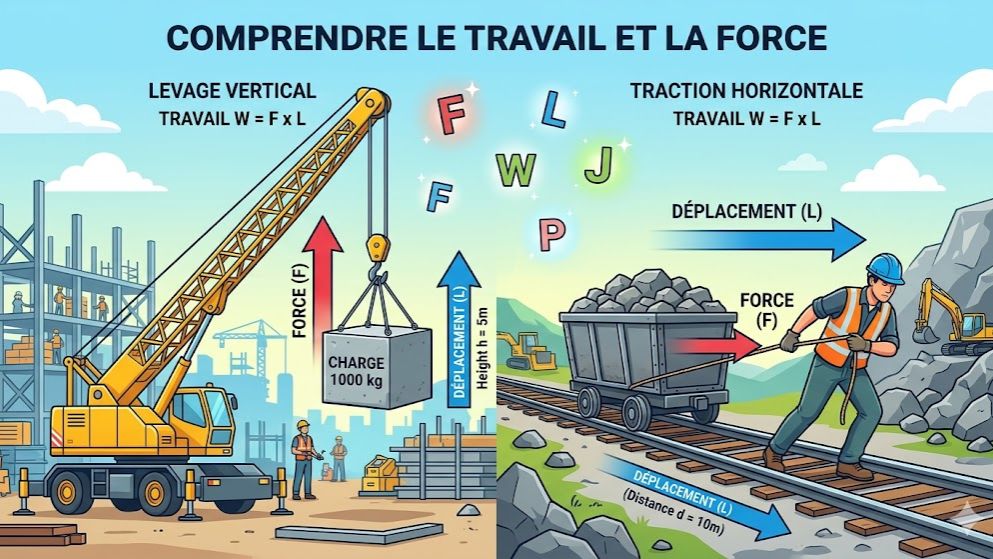
Plongez au cœur de la mécanique avec ce quiz complet dédié à la leçon sur le travail et la puissance, un pilier du programme de Physique-Chimie en classe de 3ème. Ce test interactif a été conçu pour aider les élèves à comprendre comment une force produit un effet utile lors d'un déplacement. Vous explorerez la définition mathématique du travail d'une force constante ($W = F \times L$) et apprendrez à manipuler le Joule ($J$), l'unité internationale de l'énergie. Le quiz distingue clairement le travail moteur, qui favorise le mouvement, du travail résistant, qui s'y oppose, comme c'est le cas pour les forces de frottement.
En plus du concept de travail, cette évaluation approfondit la notion de puissance mécanique ($P = W / t$). La puissance est un indicateur crucial de performance, permettant de mesurer l'efficacité d'un moteur ou d'un effort physique dans le temps. En maîtrisant le Watt ($W$), l'unité de puissance, vous serez capable de comparer la rapidité avec laquelle un travail est effectué. Ce contenu riche en explications détaillées est un atout majeur pour les révisions ciblées pour le BEPC. Testez vos capacités de calcul et consolidez vos bases scientifiques dès maintenant !
📝 Résumé de la Leçon : Travail et Puissance Mécaniques
1. Le Travail Mécanique ($W$)
Une force effectue un travail lorsque son point d'application se déplace. Si l'objet reste immobile, le travail est nul.
- Formule : $$W = F \times L$$
$W$ : Travail en Joules (J).
$F$ : Intensité de la force en Newtons (N).
$L$ : Distance du déplacement en mètres (m).
2. Travail Moteur vs Travail Résistant
- Travail Moteur ($W > 0$) : La force favorise le mouvement (elle est dans le même sens que le déplacement). Exemple : Le poids d'un objet qui descend.
- Travail Résistant ($W < 0$) : La force s'oppose au mouvement (sens contraire au déplacement). Exemple : Les forces de frottement ou le poids d'un objet que l'on monte.
3. La Puissance Mécanique ($P$)
La puissance mesure la rapidité avec laquelle un travail est effectué. Plus un travail est fait rapidement, plus la puissance est grande.
- Formules :
$$P = \frac{W}{t}$$ (où $t$ est la durée en secondes).
$$P = F \times v$$ (où $v$ est la vitesse).
- Unité : L'unité légale est le Watt (W).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité légale du travail ? | Le Joule (J). |
| Quelle est l'unité légale de la puissance ? | Le Watt (W). |
| Quelle est la formule du travail ? | $W = F \times L$. |
| Qu'est-ce qu'un travail moteur ? | Un travail où la force aide le mouvement ($W > 0$). |
| Un poids qui monte fait-il un travail moteur ? | Non, c'est un travail résistant car il s'oppose à la montée. |
| Comment calcule-t-on la puissance ? | $P = \frac{W}{t}$ ou $P = F \times v$. |
| Si le déplacement $L = 0$, que vaut le travail ? | Le travail est nul ($0$ J). |
| Que représente 1 Watt ? | C'est un travail de 1 Joule effectué en 1 seconde. |
En plus du concept de travail, cette évaluation approfondit la notion de puissance mécanique ($P = W / t$). La puissance est un indicateur crucial de performance, permettant de mesurer l'efficacité d'un moteur ou d'un effort physique dans le temps. En maîtrisant le Watt ($W$), l'unité de puissance, vous serez capable de comparer la rapidité avec laquelle un travail est effectué. Ce contenu riche en explications détaillées est un atout majeur pour les révisions ciblées pour le BEPC. Testez vos capacités de calcul et consolidez vos bases scientifiques dès maintenant !
📝 Résumé de la Leçon : Travail et Puissance Mécaniques
1. Le Travail Mécanique ($W$)
Une force effectue un travail lorsque son point d'application se déplace. Si l'objet reste immobile, le travail est nul.
- Formule : $$W = F \times L$$
$W$ : Travail en Joules (J).
$F$ : Intensité de la force en Newtons (N).
$L$ : Distance du déplacement en mètres (m).
2. Travail Moteur vs Travail Résistant
- Travail Moteur ($W > 0$) : La force favorise le mouvement (elle est dans le même sens que le déplacement). Exemple : Le poids d'un objet qui descend.
- Travail Résistant ($W < 0$) : La force s'oppose au mouvement (sens contraire au déplacement). Exemple : Les forces de frottement ou le poids d'un objet que l'on monte.
3. La Puissance Mécanique ($P$)
La puissance mesure la rapidité avec laquelle un travail est effectué. Plus un travail est fait rapidement, plus la puissance est grande.
- Formules :
$$P = \frac{W}{t}$$ (où $t$ est la durée en secondes).
$$P = F \times v$$ (où $v$ est la vitesse).
- Unité : L'unité légale est le Watt (W).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité légale du travail ? | Le Joule (J). |
| Quelle est l'unité légale de la puissance ? | Le Watt (W). |
| Quelle est la formule du travail ? | $W = F \times L$. |
| Qu'est-ce qu'un travail moteur ? | Un travail où la force aide le mouvement ($W > 0$). |
| Un poids qui monte fait-il un travail moteur ? | Non, c'est un travail résistant car il s'oppose à la montée. |
| Comment calcule-t-on la puissance ? | $P = \frac{W}{t}$ ou $P = F \times v$. |
| Si le déplacement $L = 0$, que vaut le travail ? | Le travail est nul ($0$ J). |
| Que représente 1 Watt ? | C'est un travail de 1 Joule effectué en 1 seconde. |
15m 0.0s
10
60%
Illimité
AvancéSciences
0.0
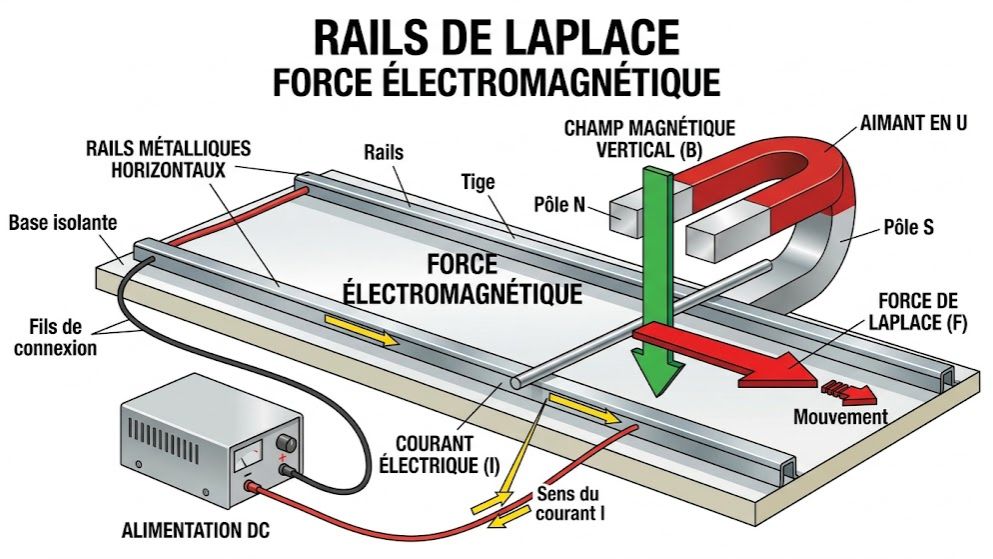
Maîtrisez les forces électromagnétiques avec ce quiz dédié à la Loi de Laplace, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre compréhension de l'interaction entre un courant électrique et un champ magnétique. Que vous soyez élève au Lycée Pierre Gadié de Yopougon ou ailleurs, révisez l'expression vectorielle de la force de Laplace $\vec{F} = I\vec{\ell} \wedge \vec{B}$ et apprenez à déterminer ses caractéristiques grâce aux règles d'orientation comme la main droite.
Le quiz couvre des applications pratiques essentielles telles que la balance de Cotton, la roue de Barlow et le fonctionnement du haut-parleur. Testez vos capacités à analyser des dispositifs expérimentaux comme les rails de Laplace. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre les fondements de la conversion d'énergie électrique en énergie mécanique avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
* Définition : Lorsqu'une tige métallique parcourue par un courant continu est plongée dans un champ magnétique, elle subit une force électromagnétique appelée force de Laplace.
* Expression vectorielle : $\vec{F} = I\vec{\ell} \wedge \vec{B}$.
* Caractéristiques de la force:
- Direction : Perpendiculaire au plan formé par le conducteur ($I\vec{\ell}$) et le champ magnétique ($\vec{B}$).
- Sens : Déterminé par la règle de la main droite, du bonhomme d'Ampère ou des trois doigts de la main droite.
- Intensité : $F = I \cdot \ell \cdot B \cdot \sin(\theta)$.
* Dispositifs expérimentaux : Les rails de Laplace et la tige de Laplace permettent de mettre en évidence cette force.
* Applications majeures : La balance de Cotton (pour mesurer $B$), la roue de Barlow et le haut-parleur.
Le quiz couvre des applications pratiques essentielles telles que la balance de Cotton, la roue de Barlow et le fonctionnement du haut-parleur. Testez vos capacités à analyser des dispositifs expérimentaux comme les rails de Laplace. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre les fondements de la conversion d'énergie électrique en énergie mécanique avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
* Définition : Lorsqu'une tige métallique parcourue par un courant continu est plongée dans un champ magnétique, elle subit une force électromagnétique appelée force de Laplace.
* Expression vectorielle : $\vec{F} = I\vec{\ell} \wedge \vec{B}$.
* Caractéristiques de la force:
- Direction : Perpendiculaire au plan formé par le conducteur ($I\vec{\ell}$) et le champ magnétique ($\vec{B}$).
- Sens : Déterminé par la règle de la main droite, du bonhomme d'Ampère ou des trois doigts de la main droite.
- Intensité : $F = I \cdot \ell \cdot B \cdot \sin(\theta)$.
* Dispositifs expérimentaux : Les rails de Laplace et la tige de Laplace permettent de mettre en évidence cette force.
* Applications majeures : La balance de Cotton (pour mesurer $B$), la roue de Barlow et le haut-parleur.
2 essai(s) il y a 6 jour(s)
10
AvancéSciences
0.0
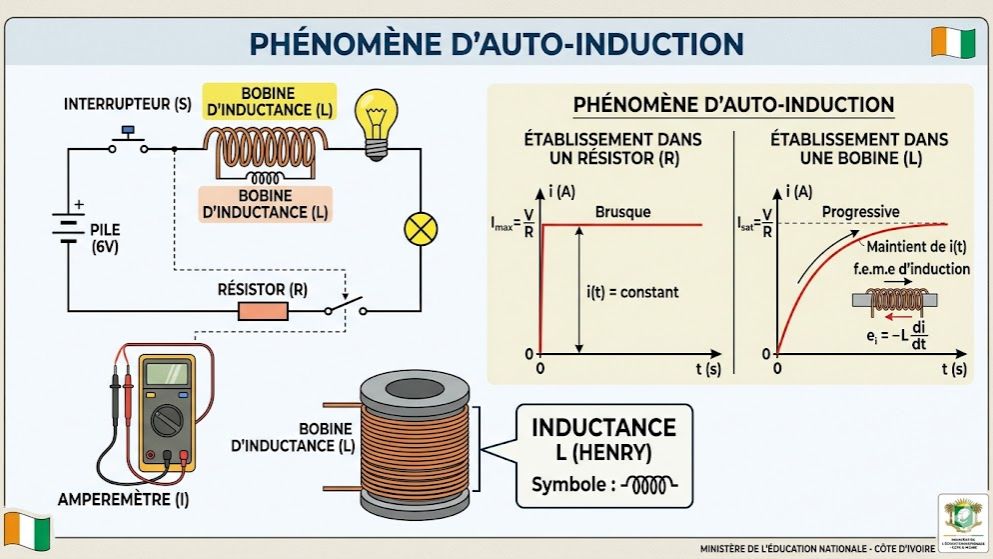
Maîtrisez les secrets de l'auto-induction avec ce quiz pédagogique conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez votre compréhension sur le comportement des bobines et des solénoïdes face aux variations de courant électrique.
Que vous soyez élève au Lycée Sainte Marie de Cocody ou dans un autre établissement, ce test vous permet de réviser des notions clés comme le flux propre $\Phi_p = L \cdot i$, l'inductance $L$ mesurée en Henry, et la force électromotrice (f.é.m.) d'auto-induction.
Apprenez à calculer l'énergie magnétique emmagasinée dans une bobine grâce à la formule $E = \frac{1}{2} L \cdot i^2$. Ce quiz aborde également des phénomènes concrets comme le retard à l'allumage des lampes fluorescentes et les étincelles de rupture. Un outil de révision optimal pour réussir votre Baccalauréat ivoirien et devenir un expert en électricité avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
- Définition :
L'auto-induction est le phénomène d'induction apparaissant dans un circuit parcouru par un courant variable, causé par la variation de son propre flux magnétique.
- Inductance ($L$) :
C'est une grandeur propre à la bobine (solénoïde), exprimée en Henry (H). Elle caractérise l'aptitude du circuit à s'opposer aux variations du courant.
- Flux propre :
Il est proportionnel à l'intensité du courant : $\Phi_p = L \cdot i$.
- Force électromotrice ($e$) :
Elle s'oppose à la variation du courant : $e = -L \cdot \frac{di}{dt}$.
- Tension aux bornes d'une bobine :
$u = L \cdot \frac{di}{dt} + r \cdot i$ (où $r$ est la résistance interne).
- Énergie emmagasinée :
Une bobine stocke de l'énergie sous forme magnétique : $E_m = \frac{1}{2} L \cdot i^2$.
Que vous soyez élève au Lycée Sainte Marie de Cocody ou dans un autre établissement, ce test vous permet de réviser des notions clés comme le flux propre $\Phi_p = L \cdot i$, l'inductance $L$ mesurée en Henry, et la force électromotrice (f.é.m.) d'auto-induction.
Apprenez à calculer l'énergie magnétique emmagasinée dans une bobine grâce à la formule $E = \frac{1}{2} L \cdot i^2$. Ce quiz aborde également des phénomènes concrets comme le retard à l'allumage des lampes fluorescentes et les étincelles de rupture. Un outil de révision optimal pour réussir votre Baccalauréat ivoirien et devenir un expert en électricité avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
- Définition :
L'auto-induction est le phénomène d'induction apparaissant dans un circuit parcouru par un courant variable, causé par la variation de son propre flux magnétique.
- Inductance ($L$) :
C'est une grandeur propre à la bobine (solénoïde), exprimée en Henry (H). Elle caractérise l'aptitude du circuit à s'opposer aux variations du courant.
- Flux propre :
Il est proportionnel à l'intensité du courant : $\Phi_p = L \cdot i$.
- Force électromotrice ($e$) :
Elle s'oppose à la variation du courant : $e = -L \cdot \frac{di}{dt}$.
- Tension aux bornes d'une bobine :
$u = L \cdot \frac{di}{dt} + r \cdot i$ (où $r$ est la résistance interne).
- Énergie emmagasinée :
Une bobine stocke de l'énergie sous forme magnétique : $E_m = \frac{1}{2} L \cdot i^2$.
2 essai(s) il y a 5 jour(s)
10
IntermédiaireSciences
0.0
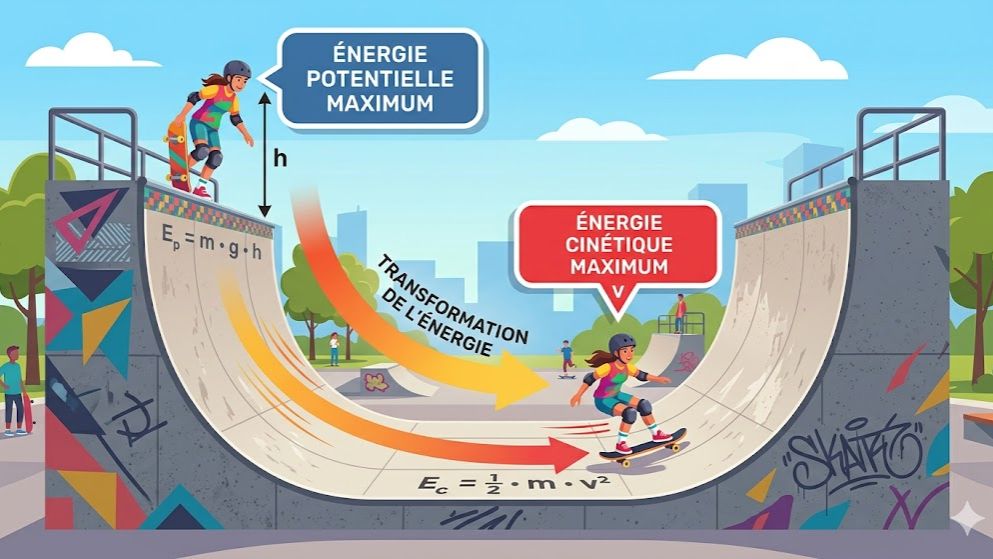
Ce quiz spécialisé traite de l'une des notions les plus importantes du programme de Physique-Chimie de 3ème : l'Énergie Mécanique. Conçu pour les élèves en Côte d'Ivoire préparant le BEPC, ce test interactif explore en détail les deux formes d'énergie qui constituent l'énergie mécanique : l'énergie cinétique ($E_c$), liée au mouvement et à la vitesse, et l'énergie potentielle de position ($E_p$), liée à l'altitude d'un corps. À travers des questions de calcul et de réflexion, vous apprendrez à utiliser les formules fondamentales comme $E_c = \frac{1}{2}mv^2$ et $E_p = mgh$.
Le quiz met un accent particulier sur le principe de conservation de l'énergie mécanique en l'absence de frottements, un concept clé pour comprendre comment l'énergie se transforme d'une forme à l'autre lors d'une chute libre ou du mouvement d'un projectile. En comprenant comment la diminution de l'énergie potentielle se traduit par une augmentation de l'énergie cinétique, vous développerez une vision globale de la dynamique des corps. Ce support pédagogique est optimisé pour offrir aux utilisateurs des explications claires et structurées qui favorisent la mémorisation et la réussite scolaire.
📝 Résumé de la Leçon : Énergie mécanique
1. L'Énergie Cinétique ($E_c$)
C'est l'énergie que possède un corps du fait de son mouvement.
- Formule : $E_c = \frac{1}{2} m \times v^2$
- Unités : $m$ en kg, $v$ en m/s et $E_c$ en Joules (J).
Note : Si la vitesse double, l'énergie cinétique est multipliée par 4 (car la vitesse est au carré).
[Image de la relation entre l'énergie cinétique, la masse et la vitesse]
2. L'Énergie Potentielle de position ($E_p$)
C'est l'énergie que possède un corps du fait de sa position (son altitude) par rapport au sol.
- Formule : $E_p = m \times g \times h$
- Unités : $m$ en kg, $g$ en N/kg (intensité de la pesanteur) et $h$ en mètres (m).
3. L'Énergie Mécanique ($E_m$)
L'énergie mécanique est la somme de l'énergie cinétique et de l'énergie potentielle.
- Formule : $E_m = E_c + E_p$
4. Conservation de l'Énergie
En l'absence de frottements (chute libre dans le vide), l'énergie mécanique d'un solide se conserve ($E_m = \text{constante}$).
- Lors d'une chute : L'altitude diminue ($E_p$ baisse) et la vitesse augmente ($E_c$ monte). L'énergie potentielle est transformée en énergie cinétique.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité internationale de l'énergie ? | Le Joule (J). |
| De quels facteurs dépend l'énergie cinétique ? | De la masse ($m$) et de la vitesse ($v$). |
| Quelle est la formule de l'énergie mécanique ? | $E_m = E_c + E_p$. |
| Un objet posé au sol a-t-il une énergie potentielle ? | Non, car sa hauteur $h = 0$, donc $E_p = 0$. |
| Que devient l'énergie mécanique sans frottements ? | Elle reste constante (elle se conserve). |
| Si un objet monte, comment évolue son $E_p$ ? | Son énergie potentielle augmente car la hauteur $h$ augmente. |
| Calcul : $m=1$ kg, $g=10$ N/kg, $h=2$ m. $E_p$ ? | $E_p = 1 \times 10 \times 2 = 20 \text{ J}$. |
| Vrai ou Faux : $E_c$ peut être négative. | Faux. Elle est toujours positive ou nulle. |
Le quiz met un accent particulier sur le principe de conservation de l'énergie mécanique en l'absence de frottements, un concept clé pour comprendre comment l'énergie se transforme d'une forme à l'autre lors d'une chute libre ou du mouvement d'un projectile. En comprenant comment la diminution de l'énergie potentielle se traduit par une augmentation de l'énergie cinétique, vous développerez une vision globale de la dynamique des corps. Ce support pédagogique est optimisé pour offrir aux utilisateurs des explications claires et structurées qui favorisent la mémorisation et la réussite scolaire.
📝 Résumé de la Leçon : Énergie mécanique
1. L'Énergie Cinétique ($E_c$)
C'est l'énergie que possède un corps du fait de son mouvement.
- Formule : $E_c = \frac{1}{2} m \times v^2$
- Unités : $m$ en kg, $v$ en m/s et $E_c$ en Joules (J).
Note : Si la vitesse double, l'énergie cinétique est multipliée par 4 (car la vitesse est au carré).
[Image de la relation entre l'énergie cinétique, la masse et la vitesse]
2. L'Énergie Potentielle de position ($E_p$)
C'est l'énergie que possède un corps du fait de sa position (son altitude) par rapport au sol.
- Formule : $E_p = m \times g \times h$
- Unités : $m$ en kg, $g$ en N/kg (intensité de la pesanteur) et $h$ en mètres (m).
3. L'Énergie Mécanique ($E_m$)
L'énergie mécanique est la somme de l'énergie cinétique et de l'énergie potentielle.
- Formule : $E_m = E_c + E_p$
4. Conservation de l'Énergie
En l'absence de frottements (chute libre dans le vide), l'énergie mécanique d'un solide se conserve ($E_m = \text{constante}$).
- Lors d'une chute : L'altitude diminue ($E_p$ baisse) et la vitesse augmente ($E_c$ monte). L'énergie potentielle est transformée en énergie cinétique.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité internationale de l'énergie ? | Le Joule (J). |
| De quels facteurs dépend l'énergie cinétique ? | De la masse ($m$) et de la vitesse ($v$). |
| Quelle est la formule de l'énergie mécanique ? | $E_m = E_c + E_p$. |
| Un objet posé au sol a-t-il une énergie potentielle ? | Non, car sa hauteur $h = 0$, donc $E_p = 0$. |
| Que devient l'énergie mécanique sans frottements ? | Elle reste constante (elle se conserve). |
| Si un objet monte, comment évolue son $E_p$ ? | Son énergie potentielle augmente car la hauteur $h$ augmente. |
| Calcul : $m=1$ kg, $g=10$ N/kg, $h=2$ m. $E_p$ ? | $E_p = 1 \times 10 \times 2 = 20 \text{ J}$. |
| Vrai ou Faux : $E_c$ peut être négative. | Faux. Elle est toujours positive ou nulle. |
2 essai(s) il y a 27 jour(s)
10
IntermédiaireSciences
0.0

Ce quiz éducatif est une ressource incontournable pour les élèves de la classe de 3ème souhaitant approfondir leurs connaissances sur le thème de l'Électricité, conformément au programme scolaire en vigueur. La leçon sur la Puissance et l'Énergie électriques est essentielle pour comprendre comment fonctionnent nos appareils domestiques, du simple téléviseur au fer à repasser. À travers ce test interactif, vous passerez en revue les formules fondamentales comme $P = U \times I$ pour la puissance en courant continu, et $E = P \times t$ pour l'énergie consommée.
Le contenu aborde également les caractéristiques nominales inscrites sur les plaques signalétiques des appareils et la distinction cruciale entre les unités légales (Watt, Joule) et les unités usuelles comme le Kilowatt-heure (kWh) utilisé par la CIE. En apprenant à calculer le coût de l'électricité et à interpréter les données d'un compteur électrique, vous développez des compétences pratiques utiles pour la vie quotidienne et pour réussir l'épreuve de Physique-Chimie au BEPC. Ce quiz sur Kwiizoo est optimisé pour offrir une expérience d'apprentissage fluide avec des explications détaillées .
📝 Résumé de la Leçon : Puissance et énergie électriques
1. La Puissance Électrique ($P$)
La puissance électrique traduit la rapidité avec laquelle un appareil transforme l'énergie.
- Expression (courant continu) : $$P = U \times I$$
- Unités : $P$ en Watts (W), $U$ en Volts (V) et $I$ en Ampères (A).
- Caractéristiques nominales : Ce sont les valeurs inscrites par le constructeur (ex: 220 V ; 100 W) pour un fonctionnement optimal.
2. L'Énergie Électrique ($E$)
L'énergie consommée par un appareil dépend de sa puissance et de sa durée d'utilisation ($t$).
- Expressions : $$E = P \times t \quad \text{ou} \quad E = U \times I \times t$$
- Unités :
- Unité légale : Le Joule (J) (quand $t$ est en secondes).
- Unité usuelle : Le Kilowattheure (kWh) ou le Wattheure (Wh) (quand $t$ est en heures).
- Conversion importante : $1 \text{ kWh} = 3\,600\,000 \text{ J}$.
3. Transformation d'énergie et Effet Joule
- Effet Joule : C'est le dégagement de chaleur lors du passage du courant dans un conducteur (ex: fer à repasser).
- Transformations : L'énergie électrique peut être transformée en énergie mécanique (moteur), thermique (chauffage) ou lumineuse (lampe).
- Facture d'électricité : Elle est établie à partir des index (ancien et nouveau) relevés sur le compteur électrique de la CIE.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité légale de la puissance ? | Le Watt (W). |
| Quelle formule lie $P$, $U$ et $I$ ? | $P = U \times I$. |
| Quelle est l'unité de l'énergie utilisée par la CIE ? | Le Kilowattheure (kWh). |
| Comment calcule-t-on l'énergie consommée ? | $E = P \times t$. |
| Qu'est-ce que l'effet Joule ? | La transformation de l'énergie électrique en chaleur. |
| Que signifie l'indication "220V" sur un appareil ? | C'est sa tension nominale de fonctionnement. |
| Comment obtenir l'intensité $I$ si on connaît $P$ et $U$ ? | $I = \frac{P}{U}$. |
| Quel appareil mesure l'énergie dans une maison ? | Le compteur électrique. |
Le contenu aborde également les caractéristiques nominales inscrites sur les plaques signalétiques des appareils et la distinction cruciale entre les unités légales (Watt, Joule) et les unités usuelles comme le Kilowatt-heure (kWh) utilisé par la CIE. En apprenant à calculer le coût de l'électricité et à interpréter les données d'un compteur électrique, vous développez des compétences pratiques utiles pour la vie quotidienne et pour réussir l'épreuve de Physique-Chimie au BEPC. Ce quiz sur Kwiizoo est optimisé pour offrir une expérience d'apprentissage fluide avec des explications détaillées .
📝 Résumé de la Leçon : Puissance et énergie électriques
1. La Puissance Électrique ($P$)
La puissance électrique traduit la rapidité avec laquelle un appareil transforme l'énergie.
- Expression (courant continu) : $$P = U \times I$$
- Unités : $P$ en Watts (W), $U$ en Volts (V) et $I$ en Ampères (A).
- Caractéristiques nominales : Ce sont les valeurs inscrites par le constructeur (ex: 220 V ; 100 W) pour un fonctionnement optimal.
2. L'Énergie Électrique ($E$)
L'énergie consommée par un appareil dépend de sa puissance et de sa durée d'utilisation ($t$).
- Expressions : $$E = P \times t \quad \text{ou} \quad E = U \times I \times t$$
- Unités :
- Unité légale : Le Joule (J) (quand $t$ est en secondes).
- Unité usuelle : Le Kilowattheure (kWh) ou le Wattheure (Wh) (quand $t$ est en heures).
- Conversion importante : $1 \text{ kWh} = 3\,600\,000 \text{ J}$.
3. Transformation d'énergie et Effet Joule
- Effet Joule : C'est le dégagement de chaleur lors du passage du courant dans un conducteur (ex: fer à repasser).
- Transformations : L'énergie électrique peut être transformée en énergie mécanique (moteur), thermique (chauffage) ou lumineuse (lampe).
- Facture d'électricité : Elle est établie à partir des index (ancien et nouveau) relevés sur le compteur électrique de la CIE.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité légale de la puissance ? | Le Watt (W). |
| Quelle formule lie $P$, $U$ et $I$ ? | $P = U \times I$. |
| Quelle est l'unité de l'énergie utilisée par la CIE ? | Le Kilowattheure (kWh). |
| Comment calcule-t-on l'énergie consommée ? | $E = P \times t$. |
| Qu'est-ce que l'effet Joule ? | La transformation de l'énergie électrique en chaleur. |
| Que signifie l'indication "220V" sur un appareil ? | C'est sa tension nominale de fonctionnement. |
| Comment obtenir l'intensité $I$ si on connaît $P$ et $U$ ? | $I = \frac{P}{U}$. |
| Quel appareil mesure l'énergie dans une maison ? | Le compteur électrique. |
6 essai(s) il y a 27 jour(s)
10
IntermédiaireSciences
0.0

Ce quiz de Physique-Chimie pour la classe de 3ème est l'outil parfait pour maîtriser le concept de conducteur ohmique, un composant électronique omniprésent dans nos appareils. À travers des questions variées et conformes au programme scolaire, vous explorerez les propriétés de la résistance électrique, son unité de mesure (l'Ohm $\Omega$) et les méthodes pour déterminer sa valeur, que ce soit par l'utilisation d'un ohmmètre ou par le code international des couleurs.
Le test met un accent particulier sur la célèbre Loi d'Ohm ($U = R \times I$), la relation fondamentale qui lie la tension à l'intensité. Vous apprendrez à interpréter la caractéristique d'un conducteur ohmique, cette droite particulière qui passe par l'origine du repère, témoignant de la proportionnalité entre $U$ et $I$. En résolvant des exercices de calcul pratiques, vous consoliderez vos bases en électricité pour briller lors de vos devoirs et réussir les épreuves du BEPC.
📝 Résumé de la Leçon : Le conducteur ohmique
1. Définition et mesure
Un conducteur ohmique (souvent appelé "résistance") est un dipôle non polarisé qui s'oppose au passage du courant électrique.
- Grandeur physique : La résistance électrique ($R$).
- Unité : L'Ohm ($\Omega$).
- Mesure : On utilise un ohmmètre (multimètre en mode $\Omega$) branché directement aux bornes du composant seul (hors circuit). On peut aussi utiliser le code international des couleurs.
[Image d'un conducteur ohmique avec ses anneaux de couleur et un multimètre]
2. La Loi d'Ohm
Pour un conducteur ohmique, la tension $U$ à ses bornes est proportionnelle à l'intensité $I$ du courant qui le traverse.
- Formule fondamentale : $$U = R \times I$$
$U$ : Tension en Volts (V).
$R$ : Résistance en Ohms ($\Omega$).
$I$ : Intensité en Ampères (A).
- Dérivées : $R = \frac{U}{I}$ et $I = \frac{U}{R}$.
3. La Caractéristique d'un conducteur ohmique
Si l'on trace le graphique de la tension $U$ en fonction de l'intensité $I$ ($U=f(I)$), on obtient une droite qui passe par l'origine du repère. Cette droite montre la proportionnalité entre $U$ et $I$. La pente (l'inclinaison) de cette droite correspond à la valeur de la résistance $R$.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité de la résistance électrique ? | L'Ohm ($\Omega$). |
| Quel appareil mesure la résistance hors circuit ? | L'ohmmètre. |
| Quelle est la formule de la loi d'Ohm ? | $U = R \times I$. |
| Quelle est la forme de la caractéristique $U=f(I)$ ? | Une droite passant par l'origine. |
| Un conducteur ohmique a-t-il un sens de branchement ? | Non, c'est un dipôle non polarisé. |
| Si $R$ augmente, que devient $I$ (à tension égale) ? | L'intensité $I$ diminue (la résistance freine le courant). |
| Calcul : $U=12$ V, $I=0,1$ A. Quelle est la valeur de $R$ ? | $R = \frac{12}{0,1} = 120 \text{ } \Omega$. |
| Comment identifier une résistance sans appareil ? | Grâce aux anneaux colorés (code des couleurs). |
Le test met un accent particulier sur la célèbre Loi d'Ohm ($U = R \times I$), la relation fondamentale qui lie la tension à l'intensité. Vous apprendrez à interpréter la caractéristique d'un conducteur ohmique, cette droite particulière qui passe par l'origine du repère, témoignant de la proportionnalité entre $U$ et $I$. En résolvant des exercices de calcul pratiques, vous consoliderez vos bases en électricité pour briller lors de vos devoirs et réussir les épreuves du BEPC.
📝 Résumé de la Leçon : Le conducteur ohmique
1. Définition et mesure
Un conducteur ohmique (souvent appelé "résistance") est un dipôle non polarisé qui s'oppose au passage du courant électrique.
- Grandeur physique : La résistance électrique ($R$).
- Unité : L'Ohm ($\Omega$).
- Mesure : On utilise un ohmmètre (multimètre en mode $\Omega$) branché directement aux bornes du composant seul (hors circuit). On peut aussi utiliser le code international des couleurs.
[Image d'un conducteur ohmique avec ses anneaux de couleur et un multimètre]
2. La Loi d'Ohm
Pour un conducteur ohmique, la tension $U$ à ses bornes est proportionnelle à l'intensité $I$ du courant qui le traverse.
- Formule fondamentale : $$U = R \times I$$
$U$ : Tension en Volts (V).
$R$ : Résistance en Ohms ($\Omega$).
$I$ : Intensité en Ampères (A).
- Dérivées : $R = \frac{U}{I}$ et $I = \frac{U}{R}$.
3. La Caractéristique d'un conducteur ohmique
Si l'on trace le graphique de la tension $U$ en fonction de l'intensité $I$ ($U=f(I)$), on obtient une droite qui passe par l'origine du repère. Cette droite montre la proportionnalité entre $U$ et $I$. La pente (l'inclinaison) de cette droite correspond à la valeur de la résistance $R$.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quelle est l'unité de la résistance électrique ? | L'Ohm ($\Omega$). |
| Quel appareil mesure la résistance hors circuit ? | L'ohmmètre. |
| Quelle est la formule de la loi d'Ohm ? | $U = R \times I$. |
| Quelle est la forme de la caractéristique $U=f(I)$ ? | Une droite passant par l'origine. |
| Un conducteur ohmique a-t-il un sens de branchement ? | Non, c'est un dipôle non polarisé. |
| Si $R$ augmente, que devient $I$ (à tension égale) ? | L'intensité $I$ diminue (la résistance freine le courant). |
| Calcul : $U=12$ V, $I=0,1$ A. Quelle est la valeur de $R$ ? | $R = \frac{12}{0,1} = 120 \text{ } \Omega$. |
| Comment identifier une résistance sans appareil ? | Grâce aux anneaux colorés (code des couleurs). |
2 essai(s) il y a 27 jour(s)
10
IntermédiaireSciences
0.0
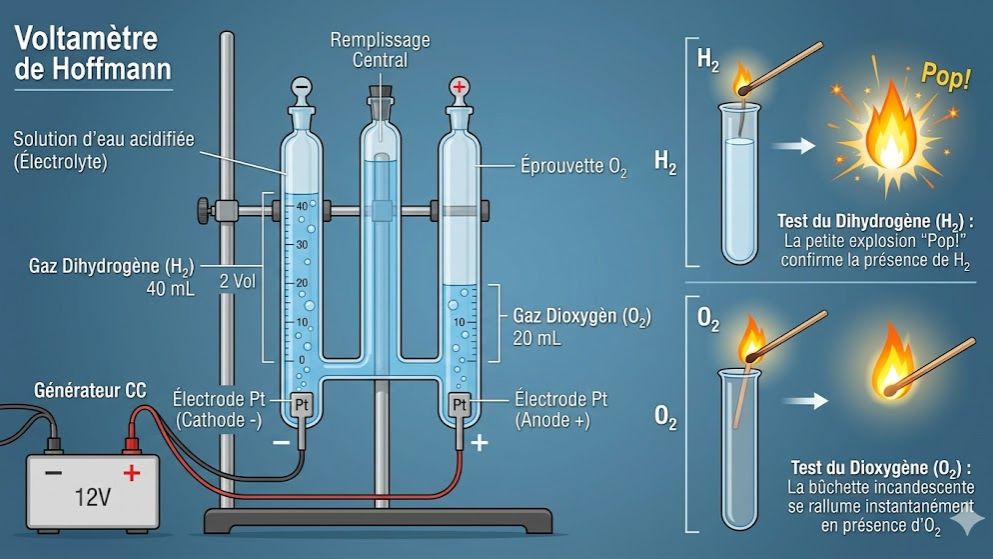
Ce quiz de Chimie, spécialement conçu pour les élèves de 3ème, explore les transformations chimiques fondamentales de l'eau ($H_2O$). À travers cette évaluation, vous maîtriserez les deux expériences clés du programme : l'électrolyse (décomposition de l'eau par le courant électrique) et la synthèse (formation de l'eau à partir de gaz). Le test couvre l'identification des gaz produits (dihydrogène et dioxygène) grâce aux tests de la flamme et de l'allumette incandescente, ainsi que les proportions volumétriques ($V(H_2) = 2 \times V(O_2)$).
Vous apprendrez à différencier l'anode de la cathode et à comprendre les équations chimiques simplifiées de ces réactions. Que vous révisiez pour un devoir en classe ou pour le BEPC, ce quiz interactif sur Kwiizoo vous offre des explications claires et rigoureuses. Ce contenu pédagogique aide les élèves à visualiser les molécules et à comprendre les bases de la chimie moléculaire tout en s'amusant. Prêt à tester vos connaissances sur les constituants de l'eau ?
📝 Résumé de la Leçon : Électrolyse et synthèse de l'eau
1. L'électrolyse de l'eau (Décomposition)
L'électrolyse est la décomposition de l'eau par le passage d'un courant électrique. Pour rendre l'eau conductrice, on y ajoute souvent un peu de soude ou d'acide.
- À l'anode (+) : Il se dégage du dioxygène ($O_2$).
- À la cathode (-) : Il se dégage du dihydrogène ($H_2$).
- Proportions : Le volume de dihydrogène produit est toujours le double de celui du dioxygène ($V_{H_2} = 2 \times V_{O_2}$).
2. Tests d'identification des gaz
- Le dihydrogène ($H_2$) : Produit une petite détonation (le fameux "Pop") à l'approche d'une flamme.
- Le dioxygène ($O_2$) : Rallume ou ravive une bûchette présentant un point incandescent.
3. La synthèse de l'eau
La synthèse est l'opération inverse de l'électrolyse : c'est la formation d'eau à partir de la réaction entre le dihydrogène et le dioxygène.
- L'expérience : On utilise souvent un eudiomètre pour provoquer une étincelle dans un mélange de ces deux gaz.
- Équation-bilan simplifiée :
$$\text{Dihydrogène} + \text{Dioxygène} \longrightarrow \text{Eau}$$
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Que signifie "Électrolyse" ? | Décomposition par l'électricité. |
| Quel gaz se forme à la cathode (-)? | Le dihydrogène ($H_2$). |
| Quel gaz se forme à l'anode (+)? | Le dioxygène ($O_2$). |
| Si j'ai 5 cm³ de $O_2$, quel est le volume de $H_2$ ? | 10 cm³ ($V_{H_2} = 2 \times V_{O_2}$). |
| Quel gaz provoque un "Pop" avec une flamme ? | Le dihydrogène. |
| Quel est le rôle du dioxygène sur une flamme ? | Il la ravive (il est comburant). |
| Quels sont les réactifs de la synthèse de l'eau ? | Le dihydrogène et le dioxygène. |
| Quel appareil utilise-t-on pour la synthèse ? | Un eudiomètre. |
Vous apprendrez à différencier l'anode de la cathode et à comprendre les équations chimiques simplifiées de ces réactions. Que vous révisiez pour un devoir en classe ou pour le BEPC, ce quiz interactif sur Kwiizoo vous offre des explications claires et rigoureuses. Ce contenu pédagogique aide les élèves à visualiser les molécules et à comprendre les bases de la chimie moléculaire tout en s'amusant. Prêt à tester vos connaissances sur les constituants de l'eau ?
📝 Résumé de la Leçon : Électrolyse et synthèse de l'eau
1. L'électrolyse de l'eau (Décomposition)
L'électrolyse est la décomposition de l'eau par le passage d'un courant électrique. Pour rendre l'eau conductrice, on y ajoute souvent un peu de soude ou d'acide.
- À l'anode (+) : Il se dégage du dioxygène ($O_2$).
- À la cathode (-) : Il se dégage du dihydrogène ($H_2$).
- Proportions : Le volume de dihydrogène produit est toujours le double de celui du dioxygène ($V_{H_2} = 2 \times V_{O_2}$).
2. Tests d'identification des gaz
- Le dihydrogène ($H_2$) : Produit une petite détonation (le fameux "Pop") à l'approche d'une flamme.
- Le dioxygène ($O_2$) : Rallume ou ravive une bûchette présentant un point incandescent.
3. La synthèse de l'eau
La synthèse est l'opération inverse de l'électrolyse : c'est la formation d'eau à partir de la réaction entre le dihydrogène et le dioxygène.
- L'expérience : On utilise souvent un eudiomètre pour provoquer une étincelle dans un mélange de ces deux gaz.
- Équation-bilan simplifiée :
$$\text{Dihydrogène} + \text{Dioxygène} \longrightarrow \text{Eau}$$
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Que signifie "Électrolyse" ? | Décomposition par l'électricité. |
| Quel gaz se forme à la cathode (-)? | Le dihydrogène ($H_2$). |
| Quel gaz se forme à l'anode (+)? | Le dioxygène ($O_2$). |
| Si j'ai 5 cm³ de $O_2$, quel est le volume de $H_2$ ? | 10 cm³ ($V_{H_2} = 2 \times V_{O_2}$). |
| Quel gaz provoque un "Pop" avec une flamme ? | Le dihydrogène. |
| Quel est le rôle du dioxygène sur une flamme ? | Il la ravive (il est comburant). |
| Quels sont les réactifs de la synthèse de l'eau ? | Le dihydrogène et le dioxygène. |
| Quel appareil utilise-t-on pour la synthèse ? | Un eudiomètre. |
3 essai(s) il y a 27 jour(s)
10
IntermédiaireSciences
0.0
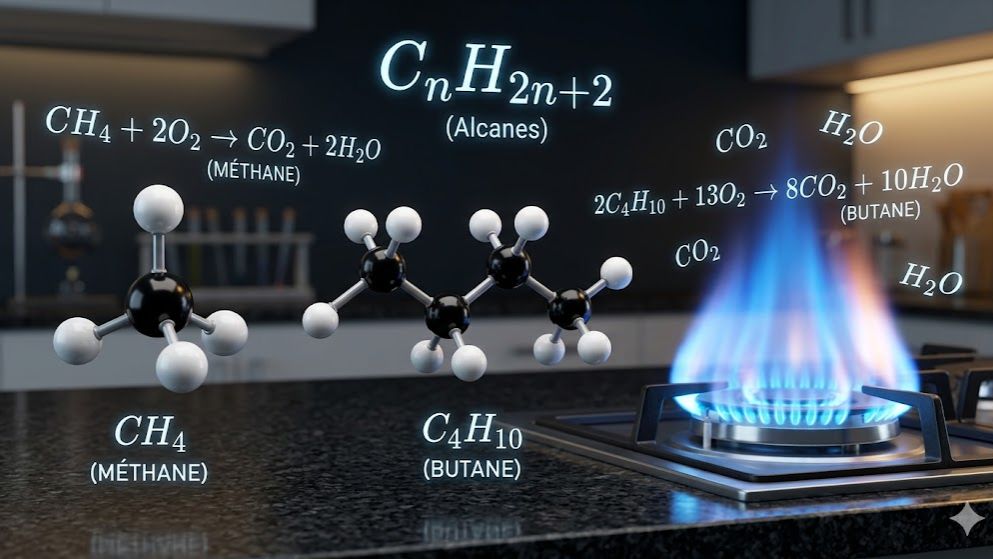
Ce quiz pédagogique est une ressource essentielle pour les élèves de 3ème souhaitant approfondir leurs connaissances sur les alcanes, une famille fondamentale d'hydrocarbures. À travers ce test, vous réviserez la définition des alcanes comme composés saturés formés uniquement d'atomes de carbone et d'hydrogène. Le quiz couvre la formule générale des alcanes ($C_n H_{2n+2}$), la nomenclature des quatre premiers membres de la famille (méthane, éthane, propane, butane) et l'étude de leurs propriétés physiques.
Une partie importante est consacrée à la réaction chimique de combustion. Vous apprendrez à distinguer la combustion complète, produisant du dioxyde de carbone ($CO_2$) et de l'eau ($H_2O$), de la combustion incomplète, dangereuse en raison de la formation de monoxyde de carbone ($CO$). Ce contenu, aligné sur le programme de Physique-Chimie de Côte d'Ivoire, est idéal pour préparer vos évaluations. Optimisé pour Kwiizoo, ce quiz propose des explications détaillées pour chaque réponse, favorisant un apprentissage autonome.
📝 Résumé de la Leçon : Les alcanes
1. Définition
Les alcanes sont des hydrocarbures saturés. Cela signifie qu'ils sont composés uniquement d'atomes de carbone ($C$) et d'hydrogène ($H$) liés par des liaisons simples.
2. Formule générale et Nomenclature
La formule générale des alcanes est : $C_nH_{2n+2}$ (où $n$ est le nombre de carbones).
Voici les quatre premiers membres de la famille :
- n = 1 : Méthane ($CH_4$)
- n = 2 : Éthane ($C_2H_6$)
- n = 3 : Propane ($C_3H_8$)
- n = 4 : Butane ($C_4H_{10}$)
[Image de la structure moléculaire des quatre premiers alcanes : méthane, éthane, propane, butane]
3. La Combustion des alcanes
C'est une réaction chimique entre l'alcane et le dioxygène ($O_2$).
- Combustion complète : Elle a lieu quand le dioxygène est en excès (flamme bleue). Elle produit du dioxyde de carbone ($CO_2$) et de l'eau ($H_2O$).
- Combustion incomplète : Elle a lieu quand le dioxygène est insuffisant (flamme jaune). Elle peut produire du carbone (suie noire) et du monoxyde de carbone ($CO$), un gaz toxique incolore et inodore.
[Image montrant la différence entre une flamme de combustion complète bleue et une flamme de combustion incomplète jaune]
4. Tests d'identification
- Eau de chaux : Se trouble en présence de $CO_2$.
- Sulfate de cuivre anhydre : Devient bleu au contact de l'eau ($H_2O$).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quels atomes composent un hydrocarbure ? | Uniquement le Carbone ($C$) et l'Hydrogène ($H$). |
| Quelle est la formule générale des alcanes ? | $C_nH_{2n+2}$. |
| Comment s'appelle l'alcane à 3 carbones ? | Le Propane. |
| Quels sont les produits d'une combustion complète ? | Le dioxyde de carbone ($CO_2$) et l'eau ($H_2O$). |
| Pourquoi la combustion incomplète est-elle dangereuse ? | Car elle produit du monoxyde de carbone ($CO$), un gaz mortel. |
| Comment identifier le $CO_2$ ? | On utilise l'eau de chaux qui devient laiteuse. |
| Quel est le constituant principal du gaz naturel ? | Le méthane ($CH_4$). |
| Que signifie un hydrocarbure "saturé" ? | Il ne possède que des liaisons simples entre les atomes de carbone. |
Une partie importante est consacrée à la réaction chimique de combustion. Vous apprendrez à distinguer la combustion complète, produisant du dioxyde de carbone ($CO_2$) et de l'eau ($H_2O$), de la combustion incomplète, dangereuse en raison de la formation de monoxyde de carbone ($CO$). Ce contenu, aligné sur le programme de Physique-Chimie de Côte d'Ivoire, est idéal pour préparer vos évaluations. Optimisé pour Kwiizoo, ce quiz propose des explications détaillées pour chaque réponse, favorisant un apprentissage autonome.
📝 Résumé de la Leçon : Les alcanes
1. Définition
Les alcanes sont des hydrocarbures saturés. Cela signifie qu'ils sont composés uniquement d'atomes de carbone ($C$) et d'hydrogène ($H$) liés par des liaisons simples.
2. Formule générale et Nomenclature
La formule générale des alcanes est : $C_nH_{2n+2}$ (où $n$ est le nombre de carbones).
Voici les quatre premiers membres de la famille :
- n = 1 : Méthane ($CH_4$)
- n = 2 : Éthane ($C_2H_6$)
- n = 3 : Propane ($C_3H_8$)
- n = 4 : Butane ($C_4H_{10}$)
[Image de la structure moléculaire des quatre premiers alcanes : méthane, éthane, propane, butane]
3. La Combustion des alcanes
C'est une réaction chimique entre l'alcane et le dioxygène ($O_2$).
- Combustion complète : Elle a lieu quand le dioxygène est en excès (flamme bleue). Elle produit du dioxyde de carbone ($CO_2$) et de l'eau ($H_2O$).
- Combustion incomplète : Elle a lieu quand le dioxygène est insuffisant (flamme jaune). Elle peut produire du carbone (suie noire) et du monoxyde de carbone ($CO$), un gaz toxique incolore et inodore.
[Image montrant la différence entre une flamme de combustion complète bleue et une flamme de combustion incomplète jaune]
4. Tests d'identification
- Eau de chaux : Se trouble en présence de $CO_2$.
- Sulfate de cuivre anhydre : Devient bleu au contact de l'eau ($H_2O$).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quels atomes composent un hydrocarbure ? | Uniquement le Carbone ($C$) et l'Hydrogène ($H$). |
| Quelle est la formule générale des alcanes ? | $C_nH_{2n+2}$. |
| Comment s'appelle l'alcane à 3 carbones ? | Le Propane. |
| Quels sont les produits d'une combustion complète ? | Le dioxyde de carbone ($CO_2$) et l'eau ($H_2O$). |
| Pourquoi la combustion incomplète est-elle dangereuse ? | Car elle produit du monoxyde de carbone ($CO$), un gaz mortel. |
| Comment identifier le $CO_2$ ? | On utilise l'eau de chaux qui devient laiteuse. |
| Quel est le constituant principal du gaz naturel ? | Le méthane ($CH_4$). |
| Que signifie un hydrocarbure "saturé" ? | Il ne possède que des liaisons simples entre les atomes de carbone. |
2 essai(s) il y a 26 jour(s)
10
IntermédiaireSciences
0.0
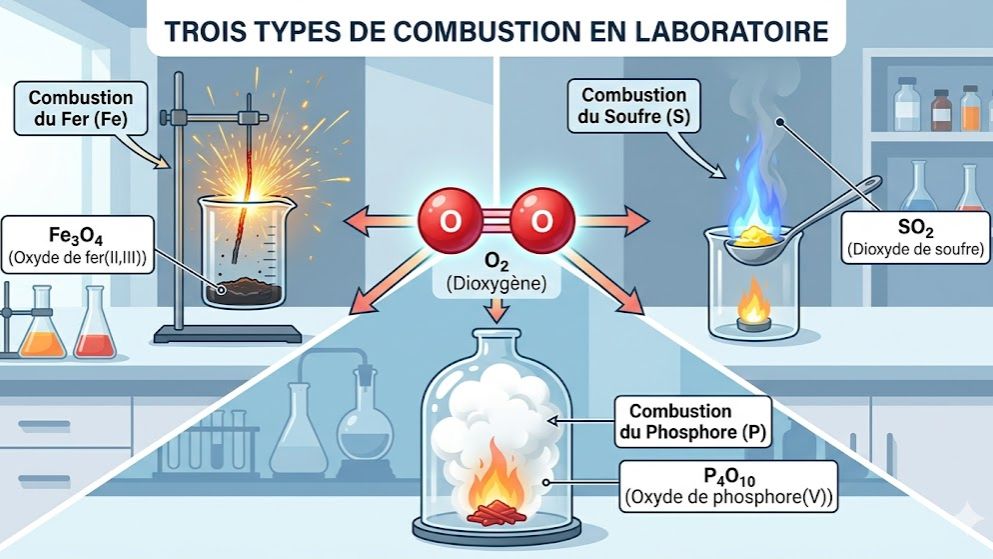
Ce quiz de Chimie pour la classe de 3ème vous plonge au cœur des réactions d'oxydation, un chapitre essentiel du programme de Physique-Chimie. À travers des questions ciblées, vous réviserez comment le dioxygène ($O_2$) réagit avec les métaux (fer, cuivre, aluminium) et les non-métaux (carbone, soufre, phosphore). Le test couvre les produits de ces réactions, tels que l'oxyde magnétique de fer ($Fe_3O_4$), l'alumine ($Al_2O_3$), ou encore le pentoxyde de phosphore ($P_2O_5$).
Vous apprendrez à identifier les caractéristiques physiques de ces oxydes (couleurs, odeurs, fumées) et à maîtriser les équations bilans simplifiées. Le quiz aborde également la distinction entre l'oxydation lente et la combustion vive, ainsi que le rôle indispensable du comburant. Ce support pédagogique sur Kwiizoo offre des explications rigoureuses pour préparer efficacement le BEPC tout en comprenant des phénomènes concrets comme la formation de la rouille ou la combustion du charbon.
📝 Résumé de la Leçon : Oxydation des corps purs simples
1. Définition générale
L'oxydation est une réaction chimique au cours de laquelle un corps pur simple se combine avec le dioxygène ($O_2$).
- Le combustible : C'est le corps qui brûle (fer, carbone, etc.).
- Le comburant : C'est le corps qui permet la combustion (le dioxygène $O_2$).
2. Oxydation des métaux (Corps simples métalliques)
Les métaux réagissent avec le dioxygène pour former des oxydes métalliques.
| Métal | Produit de l'oxydation | Observation / Caractéristique |
| Fer ($Fe$) | Oxyde magnétique ($Fe_3O_4$) | Combustion vive : étincelles et grains noirs. |
| Cuivre ($Cu$) | Oxyde de cuivre II ($CuO$) | Le métal rougit puis se recouvre d'une couche noire. |
| Aluminium ($Al$) | Alumine ($Al_2O_3$) | Couche grisâtre protectrice et imperméable. |
3. Oxydation des non-métaux (Corps simples non-métalliques)
| Non-métal | Produit de l'oxydation | Observation / Caractéristique |
| Carbone ($C$) | Dioxyde de carbone ($CO_2$) | Pas de flamme, incandescence. Trouble l'eau de chaux. |
| Soufre ($S$) | Dioxyde de soufre ($SO_2$) | Flamme bleue, gaz à odeur suffocante. |
| Phosphore ($P$) | Pentoxyde de phosphore ($P_2O_5$) | Épaisses fumées blanches très denses. |
4. Oxydation lente vs Combustion vive
- Oxydation vive (Combustion) : Réaction rapide qui dégage de la chaleur et de la lumière (flamme ou étincelles).
- Oxydation lente : Réaction lente, sans flamme ni lumière. Exemple : formation de la rouille sur le fer en présence d'air humide.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Qu'est-ce qu'une oxydation ? | Une réaction chimique entre un corps et le dioxygène. |
| Quel est l'oxyde formé par la combustion vive du fer ? | L'oxyde magnétique de fer ($Fe_3O_4$). |
| Comment appelle-t-on le produit de l'oxydation de l'aluminium ? | L'alumine ($Al_2O_3$). |
| Quelle est la couleur de la flamme du soufre qui brûle ? | Elle est de couleur bleue. |
| Quel gaz trouble l'eau de chaux ? | Le dioxyde de carbone ($CO_2$). |
| Qu'est-ce qu'un comburant ? | Le corps qui permet la combustion (ex: le dioxygène). |
| Vrai ou Faux : La rouille est une oxydation vive. | Faux. C'est une oxydation lente à l'air humide. |
| Quelle est la formule du pentoxyde de phosphore ? | $P_2O_5$. |
Vous apprendrez à identifier les caractéristiques physiques de ces oxydes (couleurs, odeurs, fumées) et à maîtriser les équations bilans simplifiées. Le quiz aborde également la distinction entre l'oxydation lente et la combustion vive, ainsi que le rôle indispensable du comburant. Ce support pédagogique sur Kwiizoo offre des explications rigoureuses pour préparer efficacement le BEPC tout en comprenant des phénomènes concrets comme la formation de la rouille ou la combustion du charbon.
📝 Résumé de la Leçon : Oxydation des corps purs simples
1. Définition générale
L'oxydation est une réaction chimique au cours de laquelle un corps pur simple se combine avec le dioxygène ($O_2$).
- Le combustible : C'est le corps qui brûle (fer, carbone, etc.).
- Le comburant : C'est le corps qui permet la combustion (le dioxygène $O_2$).
2. Oxydation des métaux (Corps simples métalliques)
Les métaux réagissent avec le dioxygène pour former des oxydes métalliques.
| Métal | Produit de l'oxydation | Observation / Caractéristique |
| Fer ($Fe$) | Oxyde magnétique ($Fe_3O_4$) | Combustion vive : étincelles et grains noirs. |
| Cuivre ($Cu$) | Oxyde de cuivre II ($CuO$) | Le métal rougit puis se recouvre d'une couche noire. |
| Aluminium ($Al$) | Alumine ($Al_2O_3$) | Couche grisâtre protectrice et imperméable. |
3. Oxydation des non-métaux (Corps simples non-métalliques)
| Non-métal | Produit de l'oxydation | Observation / Caractéristique |
| Carbone ($C$) | Dioxyde de carbone ($CO_2$) | Pas de flamme, incandescence. Trouble l'eau de chaux. |
| Soufre ($S$) | Dioxyde de soufre ($SO_2$) | Flamme bleue, gaz à odeur suffocante. |
| Phosphore ($P$) | Pentoxyde de phosphore ($P_2O_5$) | Épaisses fumées blanches très denses. |
4. Oxydation lente vs Combustion vive
- Oxydation vive (Combustion) : Réaction rapide qui dégage de la chaleur et de la lumière (flamme ou étincelles).
- Oxydation lente : Réaction lente, sans flamme ni lumière. Exemple : formation de la rouille sur le fer en présence d'air humide.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Qu'est-ce qu'une oxydation ? | Une réaction chimique entre un corps et le dioxygène. |
| Quel est l'oxyde formé par la combustion vive du fer ? | L'oxyde magnétique de fer ($Fe_3O_4$). |
| Comment appelle-t-on le produit de l'oxydation de l'aluminium ? | L'alumine ($Al_2O_3$). |
| Quelle est la couleur de la flamme du soufre qui brûle ? | Elle est de couleur bleue. |
| Quel gaz trouble l'eau de chaux ? | Le dioxyde de carbone ($CO_2$). |
| Qu'est-ce qu'un comburant ? | Le corps qui permet la combustion (ex: le dioxygène). |
| Vrai ou Faux : La rouille est une oxydation vive. | Faux. C'est une oxydation lente à l'air humide. |
| Quelle est la formule du pentoxyde de phosphore ? | $P_2O_5$. |
1 essai(s) il y a 26 jour(s)
10
IntermédiaireSciences
0.0
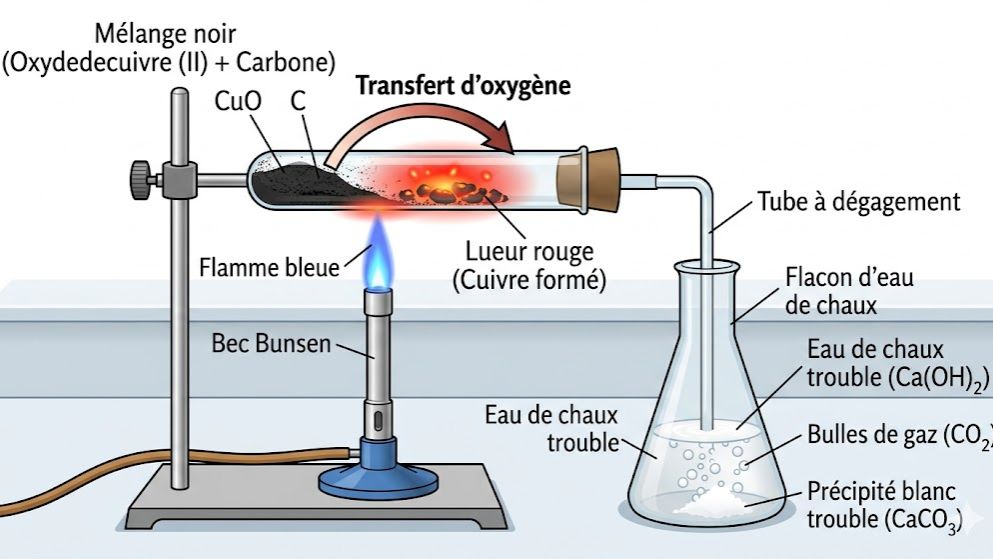
Ce quiz de Chimie pour la classe de 3ème porte sur la réduction des oxydes, un processus fondamental en métallurgie et en industrie. À travers cette évaluation, vous réviserez comment transformer un oxyde métallique (comme l'oxyde de cuivre ou l'oxyde de fer) en métal pur en utilisant des corps réducteurs tels que le carbone (charbon de bois), l'aluminium ou le dihydrogène. Le test explore en détail l'expérience classique de la réduction de l'oxyde de cuivre par le carbone, l'identification des produits formés (cuivre et dioxyde de carbone) et l'interprétation des réactions d'oxydoréduction (Redox).
Vous apprendrez à identifier le rôle du réducteur (qui capte l'oxygène) et de l'oxydant (qui cède l'oxygène). Le quiz aborde également des applications industrielles comme le fonctionnement du haut-fourneau pour la production de fer. Idéal pour préparer le BEPC, ce contenu interactif sur Kwiizoo propose des explications claires pour chaque notion, permettant aux élèves de consolider leurs bases sur les échanges d'atomes d'oxygène. Améliorez vos résultats en sciences physiques tout en découvrant les secrets de la fabrication des métaux grâce à nos explications rigoureuses et pédagogiques.
📝 Résumé de la Leçon : Réduction des oxydes
1. Définitions clés
- Réduction : C'est une réaction chimique au cours de laquelle on retire l'oxygène d'un oxyde métallique pour récupérer le métal pur.
- Réducteur : C'est le corps qui "vole" ou capte l'oxygène (ex: carbone, aluminium, dihydrogène).
- Oxydant : Dans ce contexte, c'est l'oxyde métallique qui fournit l'oxygène.
- Oxydoréduction (Redox) : C'est une réaction où une oxydation et une réduction se produisent simultanément.
2. Réduction de l'oxyde cuivrique par le carbone
C'est l'expérience de référence en classe de 3ème.
- Mélange initial : Oxyde de cuivre (noir) + Carbone (noir).
- Observations : Après chauffage, on obtient un solide rouge brique (le cuivre) et un gaz qui trouble l'eau de chaux (le dioxyde de carbone $CO_2$).
- Équation-bilan : $$2CuO + C \rightarrow 2Cu + CO_2$$
3. Autres exemples de réduction
- Réduction de l'oxyde ferrique par l'aluminium : Cette réaction (aluminothermie) produit du fer liquide et de l'alumine.
- Réduction par le dihydrogène : Le dihydrogène ($H_2$) réagit avec l'oxyde de fer pour donner du fer et de la vapeur d'eau.
Équation : $Fe_3O_4 + 4H_2 \rightarrow 3Fe + 4H_2O$
4. Application industrielle : Le Haut-fourneau
Le haut-fourneau est une installation géante utilisée en sidérurgie pour réduire les minerais de fer grâce au coke (carbone) afin de produire de la fonte.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Qu'est-ce qu'une réduction ? | C'est l'enlèvement de l'oxygène d'un oxyde. |
| Quel est le rôle du carbone dans la réduction de $CuO$ ? | Il est le réducteur (il capte l'oxygène). |
| Quelle est la couleur du cuivre métal ? | Rouge brique (ou rouge orangé). |
| Comment prouve-t-on la présence de $CO_2$ ? | Le gaz trouble l'eau de chaux. |
| Qu'est-ce qu'une réaction Redox ? | Une réaction comportant une oxydation et une réduction. |
| Qui est l'oxydant dans la réaction $CuO + C$ ? | L'oxyde de cuivre ($CuO$) car il cède l'oxygène. |
| Citez deux réducteurs autres que le carbone. | L'aluminium ($Al$) et le dihydrogène ($H_2$). |
| Où réduit-on le fer à l'échelle industrielle ? | Dans un haut-fourneau. |
Vous apprendrez à identifier le rôle du réducteur (qui capte l'oxygène) et de l'oxydant (qui cède l'oxygène). Le quiz aborde également des applications industrielles comme le fonctionnement du haut-fourneau pour la production de fer. Idéal pour préparer le BEPC, ce contenu interactif sur Kwiizoo propose des explications claires pour chaque notion, permettant aux élèves de consolider leurs bases sur les échanges d'atomes d'oxygène. Améliorez vos résultats en sciences physiques tout en découvrant les secrets de la fabrication des métaux grâce à nos explications rigoureuses et pédagogiques.
📝 Résumé de la Leçon : Réduction des oxydes
1. Définitions clés
- Réduction : C'est une réaction chimique au cours de laquelle on retire l'oxygène d'un oxyde métallique pour récupérer le métal pur.
- Réducteur : C'est le corps qui "vole" ou capte l'oxygène (ex: carbone, aluminium, dihydrogène).
- Oxydant : Dans ce contexte, c'est l'oxyde métallique qui fournit l'oxygène.
- Oxydoréduction (Redox) : C'est une réaction où une oxydation et une réduction se produisent simultanément.
2. Réduction de l'oxyde cuivrique par le carbone
C'est l'expérience de référence en classe de 3ème.
- Mélange initial : Oxyde de cuivre (noir) + Carbone (noir).
- Observations : Après chauffage, on obtient un solide rouge brique (le cuivre) et un gaz qui trouble l'eau de chaux (le dioxyde de carbone $CO_2$).
- Équation-bilan : $$2CuO + C \rightarrow 2Cu + CO_2$$
3. Autres exemples de réduction
- Réduction de l'oxyde ferrique par l'aluminium : Cette réaction (aluminothermie) produit du fer liquide et de l'alumine.
- Réduction par le dihydrogène : Le dihydrogène ($H_2$) réagit avec l'oxyde de fer pour donner du fer et de la vapeur d'eau.
Équation : $Fe_3O_4 + 4H_2 \rightarrow 3Fe + 4H_2O$
4. Application industrielle : Le Haut-fourneau
Le haut-fourneau est une installation géante utilisée en sidérurgie pour réduire les minerais de fer grâce au coke (carbone) afin de produire de la fonte.
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Qu'est-ce qu'une réduction ? | C'est l'enlèvement de l'oxygène d'un oxyde. |
| Quel est le rôle du carbone dans la réduction de $CuO$ ? | Il est le réducteur (il capte l'oxygène). |
| Quelle est la couleur du cuivre métal ? | Rouge brique (ou rouge orangé). |
| Comment prouve-t-on la présence de $CO_2$ ? | Le gaz trouble l'eau de chaux. |
| Qu'est-ce qu'une réaction Redox ? | Une réaction comportant une oxydation et une réduction. |
| Qui est l'oxydant dans la réaction $CuO + C$ ? | L'oxyde de cuivre ($CuO$) car il cède l'oxygène. |
| Citez deux réducteurs autres que le carbone. | L'aluminium ($Al$) et le dihydrogène ($H_2$). |
| Où réduit-on le fer à l'échelle industrielle ? | Dans un haut-fourneau. |
2 essai(s) il y a 26 jour(s)
10
IntermédiaireSciences
0.0
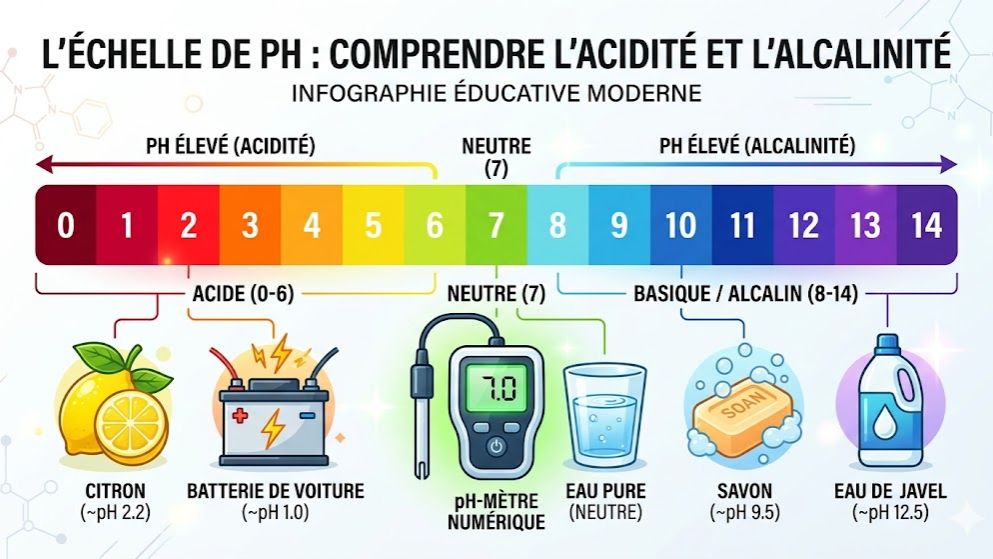
Maîtrisez l'échelle de pH avec ce quiz complet sur les solutions acides, basiques et neutres. Ce test de Physique-Chimie pour la classe de 3ème est conçu pour vous aider à comprendre comment mesurer et classer les substances chimiques que nous utilisons au quotidien. Vous réviserez l'utilisation du papier pH, du pH-mètre et des indicateurs colorés comme le Bleu de Bromothymol (BBT). Le quiz explore les propriétés des ions hydrogène ($H^+$) et hydroxyde ($OH^-$), responsables du caractère acide ou basique d'une solution.
À travers des questions pratiques, vous apprendrez à identifier les dangers des solutions concentrées et l'effet de la dilution sur la valeur du pH. Que vous soyez en train de tester l'acidité d'un jus de citron ou la basicité d'une eau savonneuse, ce contenu pédagogique vous apporte les clés pour réussir vos examens et le BEPC. Optimisé pour Kwiizoo, ce quiz propose des explications détaillées pour chaque réponse, facilitant la mémorisation des seuils critiques de l'échelle de pH (de 0 à 14) et des changements de couleurs caractéristiques des indicateurs.
📝 Résumé de la Leçon : Solutions acides, basiques et neutres
1. L'Échelle de pH
Le pH (potentiel Hydrogène) est une grandeur sans unité qui mesure le degré d'acidité ou de basicité d'une solution aqueuse. L'échelle s'étend généralement de 0 à 14.
- Solutions acides : pH < 7. Elles contiennent plus d'ions hydrogène ($H^+$) que d'ions hydroxyde ($OH^-$).
- Solutions neutres : pH = 7. Elles contiennent autant d'ions $H^+$ que d'ions $OH^-$.
- Solutions basiques : pH > 7. Elles contiennent plus d'ions hydroxyde ($OH^-$) que d'ions hydrogène ($H^+$).
2. Moyens de mesure
- Le papier pH : Change de couleur selon la solution. On compare la couleur obtenue à un nuancier pour connaître la valeur entière du pH.
- Le pH-mètre : Appareil électronique qui affiche la valeur précise du pH avec des décimales.
- Le Bleu de Bromothymol (BBT) : Un indicateur coloré qui change de couleur selon la nature de la solution :
- Jaune en milieu acide.
- Vert en milieu neutre.
- Bleu en milieu basique.
3. L'Effet de la dilution
Diluer une solution consiste à lui ajouter de l'eau distillée.
Pour une solution acide : Le pH augmente et se rapproche de 7 (elle devient moins acide).
Pour une solution basique : Le pH diminue et se rapproche de 7 (elle devient moins basique).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quel ion est responsable de l'acidité ? | L'ion hydrogène ($H^+$). |
| Quel ion est responsable de la basicité ? | L'ion hydroxyde ($OH^-$). |
| Quel est le pH d'une solution neutre ? | Le pH est égal à 7. |
| Quelle couleur prend le BBT en milieu acide ? | Il devient jaune. |
| Quel appareil donne la mesure de pH la plus précise ? | Le pH-mètre. |
| Citez deux exemples de solutions acides. | Le jus de citron et le vinaigre. |
| Que fait le pH d'une base quand on la dilue ? | Le pH diminue vers 7. |
| Une solution de pH 12 est-elle acide ou basique ? | Elle est basique (car 12 > 7). |
À travers des questions pratiques, vous apprendrez à identifier les dangers des solutions concentrées et l'effet de la dilution sur la valeur du pH. Que vous soyez en train de tester l'acidité d'un jus de citron ou la basicité d'une eau savonneuse, ce contenu pédagogique vous apporte les clés pour réussir vos examens et le BEPC. Optimisé pour Kwiizoo, ce quiz propose des explications détaillées pour chaque réponse, facilitant la mémorisation des seuils critiques de l'échelle de pH (de 0 à 14) et des changements de couleurs caractéristiques des indicateurs.
📝 Résumé de la Leçon : Solutions acides, basiques et neutres
1. L'Échelle de pH
Le pH (potentiel Hydrogène) est une grandeur sans unité qui mesure le degré d'acidité ou de basicité d'une solution aqueuse. L'échelle s'étend généralement de 0 à 14.
- Solutions acides : pH < 7. Elles contiennent plus d'ions hydrogène ($H^+$) que d'ions hydroxyde ($OH^-$).
- Solutions neutres : pH = 7. Elles contiennent autant d'ions $H^+$ que d'ions $OH^-$.
- Solutions basiques : pH > 7. Elles contiennent plus d'ions hydroxyde ($OH^-$) que d'ions hydrogène ($H^+$).
2. Moyens de mesure
- Le papier pH : Change de couleur selon la solution. On compare la couleur obtenue à un nuancier pour connaître la valeur entière du pH.
- Le pH-mètre : Appareil électronique qui affiche la valeur précise du pH avec des décimales.
- Le Bleu de Bromothymol (BBT) : Un indicateur coloré qui change de couleur selon la nature de la solution :
- Jaune en milieu acide.
- Vert en milieu neutre.
- Bleu en milieu basique.
3. L'Effet de la dilution
Diluer une solution consiste à lui ajouter de l'eau distillée.
Pour une solution acide : Le pH augmente et se rapproche de 7 (elle devient moins acide).
Pour une solution basique : Le pH diminue et se rapproche de 7 (elle devient moins basique).
🧠 Fiche de Mémorisation (Flashcards)
| Question | Réponse |
| Quel ion est responsable de l'acidité ? | L'ion hydrogène ($H^+$). |
| Quel ion est responsable de la basicité ? | L'ion hydroxyde ($OH^-$). |
| Quel est le pH d'une solution neutre ? | Le pH est égal à 7. |
| Quelle couleur prend le BBT en milieu acide ? | Il devient jaune. |
| Quel appareil donne la mesure de pH la plus précise ? | Le pH-mètre. |
| Citez deux exemples de solutions acides. | Le jus de citron et le vinaigre. |
| Que fait le pH d'une base quand on la dilue ? | Le pH diminue vers 7. |
| Une solution de pH 12 est-elle acide ou basique ? | Elle est basique (car 12 > 7). |
1 essai(s) il y a 26 jour(s)
10
Commentaires (0)
Connectez-vous pour commenter
Cliquez ici pour vous connecter