Fission, Fusion et Énergie Nucléaire (Physique-Chimie Terminale C & D - CI)
AvancéSciences
1 essai
0.0(0)
1 essai•il y a 3 jour(s)
Approfondissez vos connaissances en physique atomique avec ce quiz sur les réactions nucléaires provoquées, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test explore les mécanismes de la fission et de la fusion nucléaire, des concepts essentiels pour comprendre la production d'électricité et l'énergie des étoiles. Que vous soyez élève au Lycée Moderne 2 Pierre Gadié de Yopougon ou ailleurs, révisez les définitions du défaut de masse, de l'énergie de liaison et de l'énergie de liaison par nucléon. Apprenez à équilibrer des équations-bilans de réactions provoquées et découvrez les applications ainsi que les dangers liés à la radioactivité.
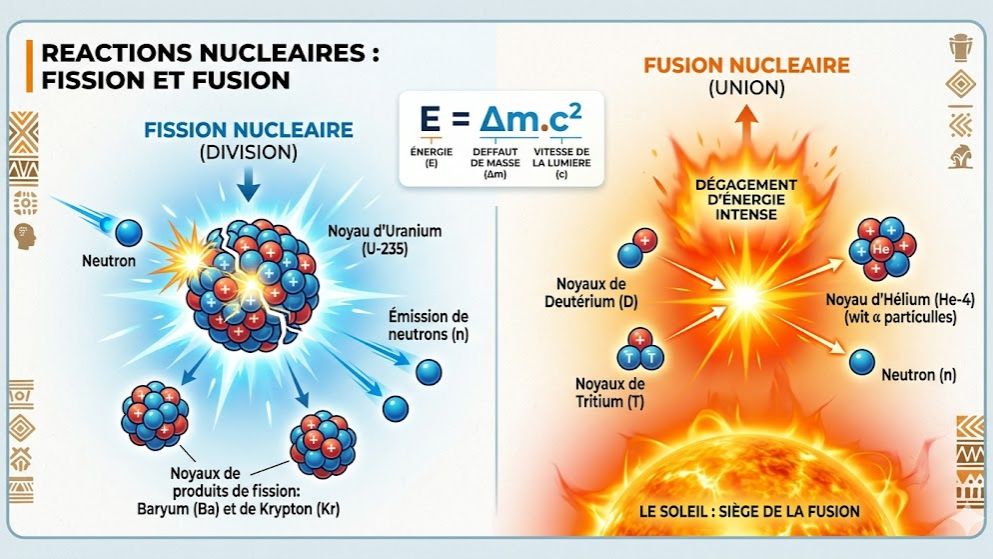
Ce quiz évalue votre maîtrise de la célèbre relation d'Einstein $E = \Delta m \cdot c^2$. Un outil de révision stratégique pour le Baccalauréat ivoirien avec Kwiizoo, votre allié pour l'excellence académique.
## Résumé du Cours (Aide-mémoire) ##
Défaut de masse ($\Delta m$) : La masse d'un noyau est toujours inférieure à la somme des masses de ses nucléons isolés.
Énergie de liaison ($E_\ell$) : Énergie qu'il faut fournir au noyau pour le séparer en nucléons isolés au repos. Elle est donnée par la relation d'Einstein : $E_\ell = \Delta m \cdot c^2$.
Fission Nucléaire : Un noyau lourd (ex: Uranium 235) se casse en deux noyaux plus légers sous l'impact d'un neutron.
Fusion Nucléaire : Deux noyaux très légers (ex: Deutérium et Tritium) s'unissent pour former un noyau plus lourd.
Stabilité : Plus l'énergie de liaison par nucléon ($E_\ell/A$) est grande, plus le noyau est stable.
Ce quiz évalue votre maîtrise de la célèbre relation d'Einstein $E = \Delta m \cdot c^2$. Un outil de révision stratégique pour le Baccalauréat ivoirien avec Kwiizoo, votre allié pour l'excellence académique.
## Résumé du Cours (Aide-mémoire) ##
Défaut de masse ($\Delta m$) : La masse d'un noyau est toujours inférieure à la somme des masses de ses nucléons isolés.
Énergie de liaison ($E_\ell$) : Énergie qu'il faut fournir au noyau pour le séparer en nucléons isolés au repos. Elle est donnée par la relation d'Einstein : $E_\ell = \Delta m \cdot c^2$.
Fission Nucléaire : Un noyau lourd (ex: Uranium 235) se casse en deux noyaux plus légers sous l'impact d'un neutron.
Fusion Nucléaire : Deux noyaux très légers (ex: Deutérium et Tritium) s'unissent pour former un noyau plus lourd.
Stabilité : Plus l'énergie de liaison par nucléon ($E_\ell/A$) est grande, plus le noyau est stable.
15m 0.0s
10
60%
Illimité
AvancéSciences
0.0
Maîtrisez les fondamentaux de la physique nucléaire avec ce quiz sur les réactions nucléaires spontanées, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez vos connaissances sur la structure du noyau atomique, les isotopes et l'unité de masse atomique.
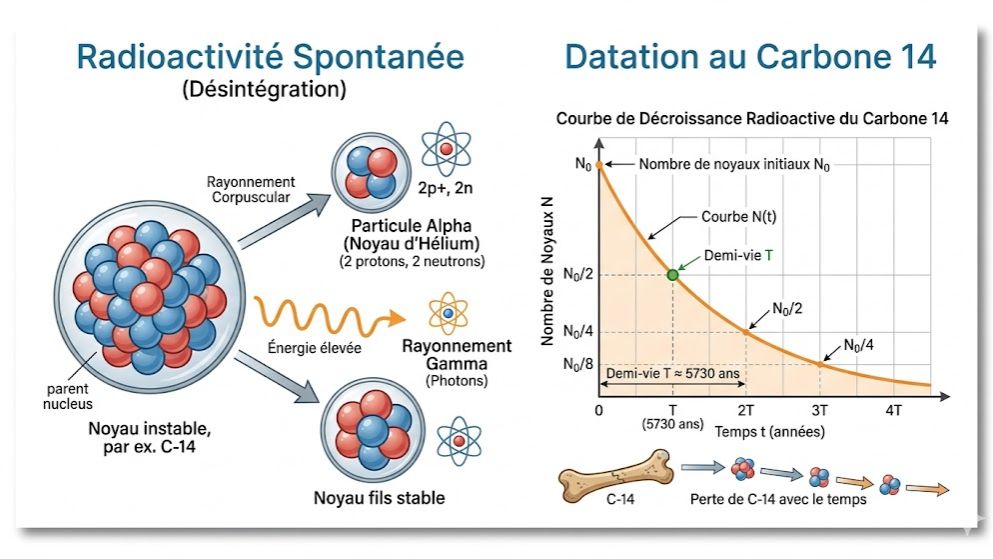
Que vous soyez élève au Lycée Moderne d’Adzopé ou ailleurs, révisez les différents types d'émissions radioactives ($\alpha, \beta$ et $\gamma$) ainsi que les lois de conservation de Soddy. Ce quiz évalue votre capacité à établir et utiliser la loi de décroissance radioactive $N = N_0 e^{-\lambda t}$ et à comprendre des concepts clés comme la demi-vie ou période radioactive. Apprenez comment les archéologues déterminent l'âge des vestiges grâce à la datation au carbone 14. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
# Nucléide et Isotopes : Un nucléide est caractérisé par son nombre de protons $Z$ et de neutrons. Les isotopes sont des nucléides ayant le même $Z$ mais des nombres de masse $A$ différents.
# Types de Radioactivité :
- $\alpha$ (alpha) : Émission d'un noyau d'Hélium $^4_2He$.
- $\beta^-$ (bêta moins) : Émission d'un électron $^0_{-1}e$.
- $\beta^+$ (bêta plus) : Émission d'un positon $^0_{1}e$.
- $\gamma$ (gamma) : Émission d'un rayonnement électromagnétique de haute énergie.
# Loi de décroissance : Le nombre de noyaux restants est $N(t) = N_0 e^{-\lambda t}$.
# Période (Demi-vie) $T$ : Durée au bout de laquelle la moitié des noyaux initiaux se sont désintégrés. Relation : $T = \frac{\ln 2}{\lambda}$.
# Activité $A$ : Nombre de désintégrations par seconde, mesuré en Becquerel (Bq).
Que vous soyez élève au Lycée Moderne d’Adzopé ou ailleurs, révisez les différents types d'émissions radioactives ($\alpha, \beta$ et $\gamma$) ainsi que les lois de conservation de Soddy. Ce quiz évalue votre capacité à établir et utiliser la loi de décroissance radioactive $N = N_0 e^{-\lambda t}$ et à comprendre des concepts clés comme la demi-vie ou période radioactive. Apprenez comment les archéologues déterminent l'âge des vestiges grâce à la datation au carbone 14. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien avec Kwiizoo.
Résumé du Cours (Aide-mémoire)
# Nucléide et Isotopes : Un nucléide est caractérisé par son nombre de protons $Z$ et de neutrons. Les isotopes sont des nucléides ayant le même $Z$ mais des nombres de masse $A$ différents.
# Types de Radioactivité :
- $\alpha$ (alpha) : Émission d'un noyau d'Hélium $^4_2He$.
- $\beta^-$ (bêta moins) : Émission d'un électron $^0_{-1}e$.
- $\beta^+$ (bêta plus) : Émission d'un positon $^0_{1}e$.
- $\gamma$ (gamma) : Émission d'un rayonnement électromagnétique de haute énergie.
# Loi de décroissance : Le nombre de noyaux restants est $N(t) = N_0 e^{-\lambda t}$.
# Période (Demi-vie) $T$ : Durée au bout de laquelle la moitié des noyaux initiaux se sont désintégrés. Relation : $T = \frac{\ln 2}{\lambda}$.
# Activité $A$ : Nombre de désintégrations par seconde, mesuré en Becquerel (Bq).
1 essai(s) il y a 3 jour(s)
10
AvancéSciences
0.0
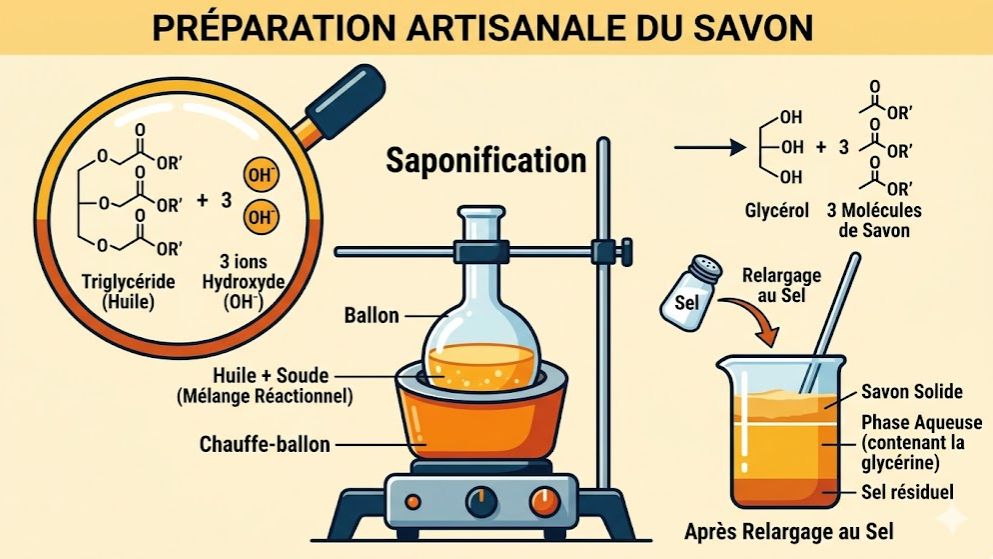
Devenez incollable sur la fabrication du savon avec ce quiz pédagogique basé sur le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. À travers ce test, révisez la réaction de saponification, un processus chimique fondamental où un corps gras (triester) réagit avec une base forte pour produire du savon et du glycérol.
Que vous soyez élève au Lycée Municipal de Williamsville ou ailleurs, ce quiz évalue votre connaissance des caractéristiques de cette réaction : elle est lente à froid, mais totale et exothermique. Apprenez à identifier la formule générale d'un savon, ses propriétés détergentes et les étapes de fabrication comme le relargage. Un outil indispensable pour maîtriser la chimie organique et réussir votre Baccalauréat avec Kwiizoo, l'application leader pour l'excellence académique ivoirienne.
## Résumé du Cours (Aide-mémoire) ##
# Définition : La saponification est l'hydrolyse en milieu basique (soude ou potasse) d'un ester, plus précisément d'un corps gras (triglycéride).
# Réaction : Corps gras + Base forte (NaOH ou KOH) $\rightarrow$ Savon + Glycérol.
# Caractéristiques : C'est une réaction lente (à température ambiante), mais totale et exothermique.
# Structure d'un savon : Un savon est un mélange de carboxylates de sodium (savon dur) ou de potassium (savon mou). Il possède une tête hydrophile (qui aime l'eau) et une queue hydrophobe/lipophile (qui aime les graisses).
# Le Relargage : Étape consistant à ajouter du sel (NaCl) pour précipiter le savon et le séparer du mélange.
Que vous soyez élève au Lycée Municipal de Williamsville ou ailleurs, ce quiz évalue votre connaissance des caractéristiques de cette réaction : elle est lente à froid, mais totale et exothermique. Apprenez à identifier la formule générale d'un savon, ses propriétés détergentes et les étapes de fabrication comme le relargage. Un outil indispensable pour maîtriser la chimie organique et réussir votre Baccalauréat avec Kwiizoo, l'application leader pour l'excellence académique ivoirienne.
## Résumé du Cours (Aide-mémoire) ##
# Définition : La saponification est l'hydrolyse en milieu basique (soude ou potasse) d'un ester, plus précisément d'un corps gras (triglycéride).
# Réaction : Corps gras + Base forte (NaOH ou KOH) $\rightarrow$ Savon + Glycérol.
# Caractéristiques : C'est une réaction lente (à température ambiante), mais totale et exothermique.
# Structure d'un savon : Un savon est un mélange de carboxylates de sodium (savon dur) ou de potassium (savon mou). Il possède une tête hydrophile (qui aime l'eau) et une queue hydrophobe/lipophile (qui aime les graisses).
# Le Relargage : Étape consistant à ajouter du sel (NaCl) pour précipiter le savon et le séparer du mélange.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
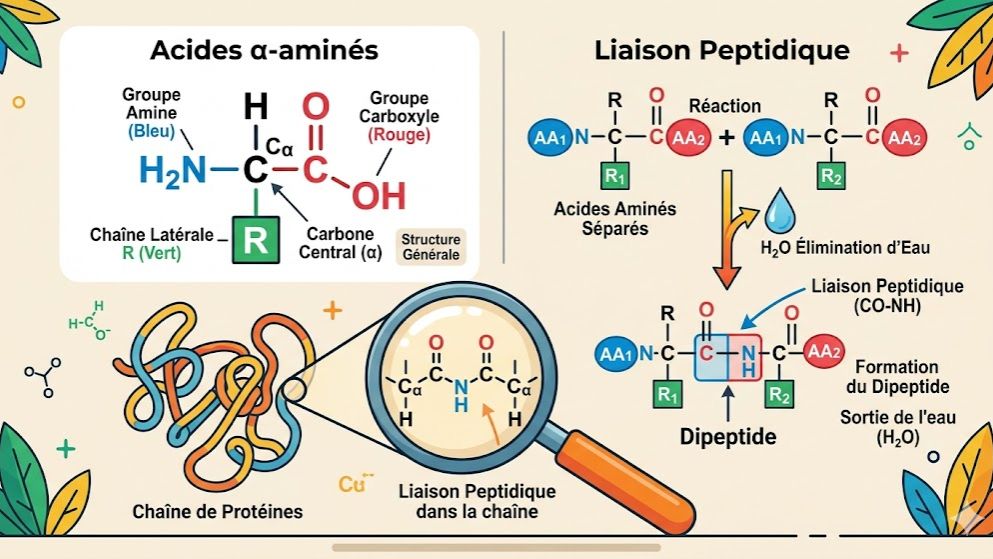
Plongez dans la chimie du vivant avec ce quiz sur les acides $\alpha$-aminés, conçu selon le programme de Physique-Chimie de la Terminale D en Côte d'Ivoire. Ce test interactif vous permet de réviser la structure bifonctionnelle de ces molécules essentielles, portant à la fois un groupe amino et un groupe carboxyle sur le même carbone.
Que vous soyez élève dans un lycée ivoirien ou passionné de biochimie, testez vos connaissances sur la nomenclature IUPAC, le caractère amphotère du zwitterion (ion dipolaire) et la formation de la liaison peptidique. Apprenez à identifier les dipeptides et les protéines, et révisez les tests caractéristiques comme la réaction du Biuret. Un outil de révision stratégique pour maîtriser ce chapitre clé du Baccalauréat ivoirien et comprendre comment notre corps construit ses propres protéines avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Définition : Un acide $\alpha$-aminé possède un groupe amine ($-NH_2$) et un groupe carboxyle ($-COOH$) fixés sur le même atome de carbone dit "carbone $\alpha$".
Structure et pH : En solution aqueuse, ils existent sous forme d'ion dipolaire appelé zwitterion ou amphion.
Propriétés amphotères : Le zwitterion se comporte comme une base en milieu acide et comme un acide en milieu basique.
Liaison Peptidique : C'est une liaison amide ($-NH-CO-$) qui se forme par élimination d'une molécule d'eau entre deux acides $\alpha$-aminés.
Protéines : Ce sont des macromolécules formées par l'enchaînement d'un grand nombre d'acides aminés (généralement plus de 50).
Identification : La réaction de Biuret permet de mettre en évidence la présence de liaisons peptidiques (coloration violette en présence d'ions $Cu^{2+}$ en milieu basique).
Que vous soyez élève dans un lycée ivoirien ou passionné de biochimie, testez vos connaissances sur la nomenclature IUPAC, le caractère amphotère du zwitterion (ion dipolaire) et la formation de la liaison peptidique. Apprenez à identifier les dipeptides et les protéines, et révisez les tests caractéristiques comme la réaction du Biuret. Un outil de révision stratégique pour maîtriser ce chapitre clé du Baccalauréat ivoirien et comprendre comment notre corps construit ses propres protéines avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Définition : Un acide $\alpha$-aminé possède un groupe amine ($-NH_2$) et un groupe carboxyle ($-COOH$) fixés sur le même atome de carbone dit "carbone $\alpha$".
Structure et pH : En solution aqueuse, ils existent sous forme d'ion dipolaire appelé zwitterion ou amphion.
Propriétés amphotères : Le zwitterion se comporte comme une base en milieu acide et comme un acide en milieu basique.
Liaison Peptidique : C'est une liaison amide ($-NH-CO-$) qui se forme par élimination d'une molécule d'eau entre deux acides $\alpha$-aminés.
Protéines : Ce sont des macromolécules formées par l'enchaînement d'un grand nombre d'acides aminés (généralement plus de 50).
Identification : La réaction de Biuret permet de mettre en évidence la présence de liaisons peptidiques (coloration violette en présence d'ions $Cu^{2+}$ en milieu basique).
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
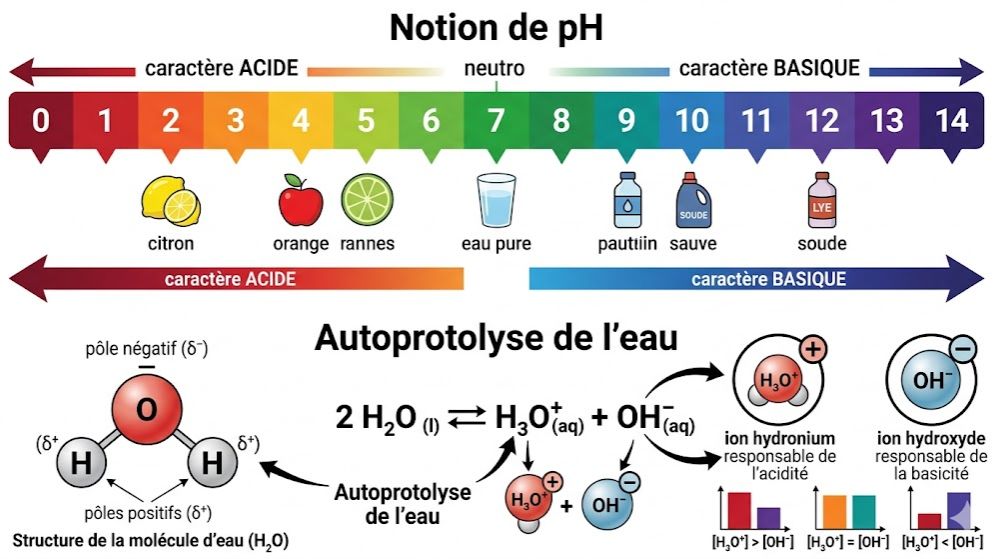
Maîtrisez les fondamentaux de la chimie des solutions avec ce quiz sur les solutions aqueuses et la notion de pH, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez vos connaissances sur les propriétés uniques de l'eau en tant que solvant dipolaire, ionisant et hydratant.
Que vous étudiiez au Lycée Moderne d’Azaguié ou ailleurs, ce test vous permet de réviser l'équation d'autoprotolyse de l'eau , le produit ionique $K_e$ et la définition logarithmique du pH. Évaluez votre capacité à vérifier l'électroneutralité d'une solution et à calculer les concentrations molaires des espèces chimiques présentes. Apprenez à classer les solutions en fonction de leur acidité ou basicité et comprenez les limites de validité de la relation pH = -log[H3O+]. Un outil de révision essentiel pour réussir le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
L'Eau, un solvant particulier : Molécule polaire capable de disloquer, d'ioniser et d'hydrater les solutés.
Autoprotolyse de l'eau : Réaction entre deux molécules d'eau produisant des ions hydronium et hydroxyde : $2H_2O \rightleftharpoons H_3O^+ + OH^-$.
Produit ionique ($K_e$) : À 25°C, $K_e = [H_3O^+][OH^-] = 10^{-14}$.
Définition du pH : $pH = -\log[H_3O^+]$. Cette relation est valable pour des solutions diluées ($C \le 0,1 \text{ mol/L}$).
Lois de conservation :
- Électroneutralité : La somme des charges positives est égale à la somme des charges négatives.
- Conservation de la matière : La quantité de matière de l'élément chimique se conserve lors de la dissolution.
Que vous étudiiez au Lycée Moderne d’Azaguié ou ailleurs, ce test vous permet de réviser l'équation d'autoprotolyse de l'eau , le produit ionique $K_e$ et la définition logarithmique du pH. Évaluez votre capacité à vérifier l'électroneutralité d'une solution et à calculer les concentrations molaires des espèces chimiques présentes. Apprenez à classer les solutions en fonction de leur acidité ou basicité et comprenez les limites de validité de la relation pH = -log[H3O+]. Un outil de révision essentiel pour réussir le Baccalauréat ivoirien avec Kwiizoo !
## Résumé du Cours (Aide-mémoire) ##
L'Eau, un solvant particulier : Molécule polaire capable de disloquer, d'ioniser et d'hydrater les solutés.
Autoprotolyse de l'eau : Réaction entre deux molécules d'eau produisant des ions hydronium et hydroxyde : $2H_2O \rightleftharpoons H_3O^+ + OH^-$.
Produit ionique ($K_e$) : À 25°C, $K_e = [H_3O^+][OH^-] = 10^{-14}$.
Définition du pH : $pH = -\log[H_3O^+]$. Cette relation est valable pour des solutions diluées ($C \le 0,1 \text{ mol/L}$).
Lois de conservation :
- Électroneutralité : La somme des charges positives est égale à la somme des charges négatives.
- Conservation de la matière : La quantité de matière de l'élément chimique se conserve lors de la dissolution.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
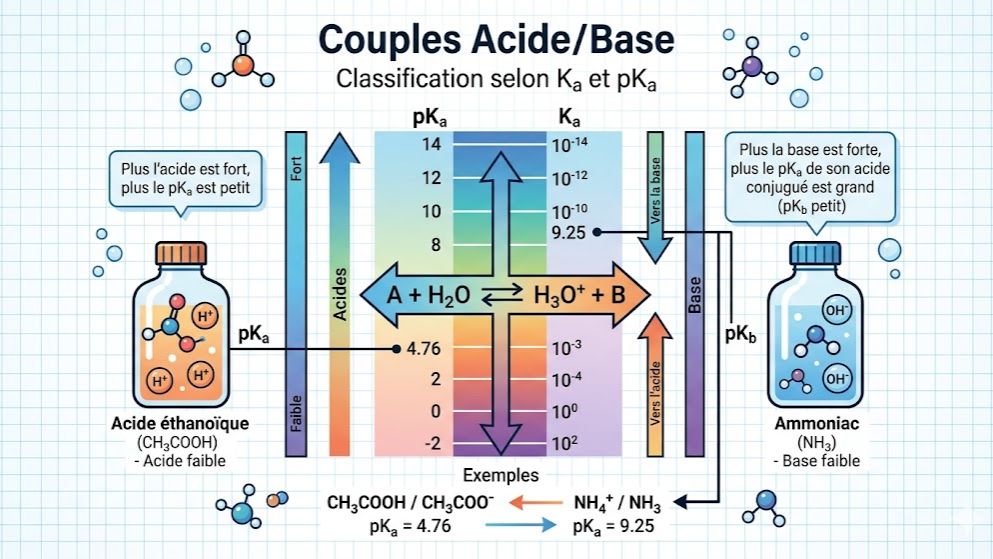
Maîtrisez la force relative des acides et des bases avec ce quiz sur les couples acido-basiques, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre compréhension des définitions de Brönsted et votre capacité à identifier les acides et leurs bases conjuguées.
Que vous soyez élève au Lycée Moderne d’Agnibilékrou ou ailleurs, ce quiz vous permet de réviser les constantes d'acidité $K_A$ et le $pK_A$, outils indispensables pour classer les couples selon leur force. Apprenez à déterminer les domaines de prédominance et à choisir le bon indicateur coloré grâce à sa zone de virage. Évaluez vos compétences sur la relation $pH = pK_A + \log([B]/[A])$ et comprenez pourquoi certains acides sont plus forts que d'autres. Un entraînement idéal pour réussir le Baccalauréat ivoirien et exceller en chimie générale avec Kwiizoo.
## Résumé du Cours (Aide-mémoire). ##
Définition de Brönsted : Un acide est une espèce capable de céder un proton $H^+$ ; une base est une espèce capable d'en capter un.
Couple Acide/Base : Formé par deux espèces qui se transforment l'une en l'autre par gain ou perte d'un proton.
Constante d'acidité ($K_A$) : Grandeur caractérisant la force d'un acide dans l'eau. Plus le $K_A$ est grand (ou le $pK_A$ petit), plus l'acide est fort.
Relation fondamentale : $pH = pK_A + \log \frac{[\text{Base}]}{[\text{Acide}]}$.
Domaine de prédominance :
- Si $pH < pK_A$ : l'Acide prédomine.
- Si $pH > pK_A$ : la Base prédomine.
Que vous soyez élève au Lycée Moderne d’Agnibilékrou ou ailleurs, ce quiz vous permet de réviser les constantes d'acidité $K_A$ et le $pK_A$, outils indispensables pour classer les couples selon leur force. Apprenez à déterminer les domaines de prédominance et à choisir le bon indicateur coloré grâce à sa zone de virage. Évaluez vos compétences sur la relation $pH = pK_A + \log([B]/[A])$ et comprenez pourquoi certains acides sont plus forts que d'autres. Un entraînement idéal pour réussir le Baccalauréat ivoirien et exceller en chimie générale avec Kwiizoo.
## Résumé du Cours (Aide-mémoire). ##
Définition de Brönsted : Un acide est une espèce capable de céder un proton $H^+$ ; une base est une espèce capable d'en capter un.
Couple Acide/Base : Formé par deux espèces qui se transforment l'une en l'autre par gain ou perte d'un proton.
Constante d'acidité ($K_A$) : Grandeur caractérisant la force d'un acide dans l'eau. Plus le $K_A$ est grand (ou le $pK_A$ petit), plus l'acide est fort.
Relation fondamentale : $pH = pK_A + \log \frac{[\text{Base}]}{[\text{Acide}]}$.
Domaine de prédominance :
- Si $pH < pK_A$ : l'Acide prédomine.
- Si $pH > pK_A$ : la Base prédomine.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
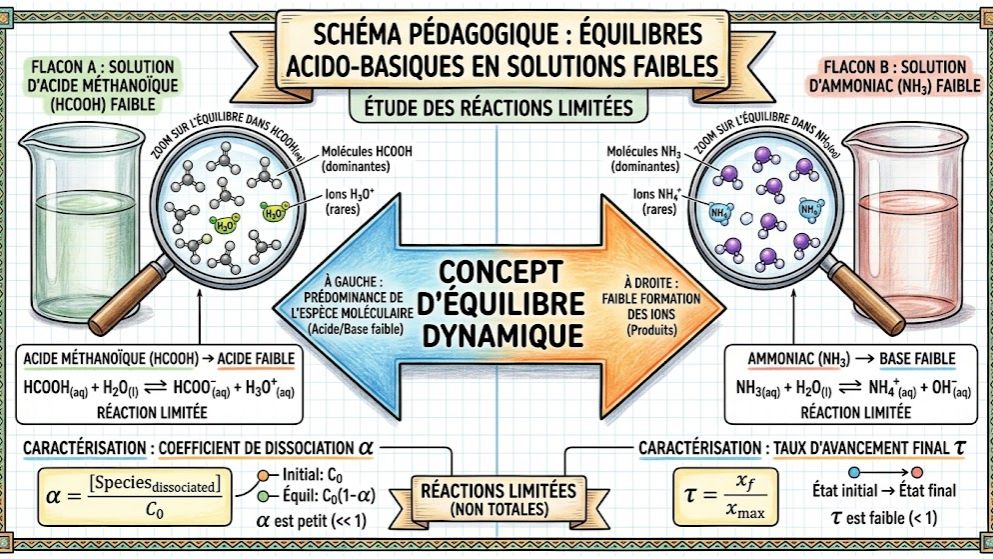
Maîtrisez les concepts d'équilibre chimique avec ce quiz sur les acides et bases faibles, conforme au programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez votre compréhension sur la réaction partielle de l'acide éthanoïque ou de l'ammoniac avec l'eau.
Que vous soyez élève au Lycée Moderne de Bangolo ou ailleurs, ce test vous permet de réviser des notions clés comme le coefficient d'ionisation ($\alpha$), l'équilibre chimique et l'effet de la dilution sur l'ionisation des espèces. Évaluez votre capacité à calculer les concentrations molaires des espèces chimiques présentes dans une solution faible et à interpréter les différences de pH entre solutions de même concentration. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien et maîtriser la chimie générale avec Kwiizoo.
1. Définitions Fondamentales
. Acide Faible : Espèce chimique dont la réaction avec l’eau est partielle (ou limitée).
Équation : $AH + H_2O \rightleftharpoons A^- + H_3O^+$
Exemple : L’acide éthanoïque ($CH_3COOH$).
. Base Faible : Espèce dont la réaction avec l’eau est incomplète.
Équation : $B + H_2O \rightleftharpoons BH^+ + OH^-$
Exemple : L’ammoniac ($NH_3$).
2. Le Coefficient d'Ionisation ($\alpha$)
C'est un élément clé de la page 29 du programme ivoirien.
. Formule : $\alpha = \frac{\text{quantité d'acide réagi}}{\text{quantité d'acide initial}}$
. Propriété : Pour un acide faible, $0 < \alpha < 1$. Plus la solution est diluée, plus $\alpha$ augmente (loi de dilution d'Ostwald).
3. Étude Quantitative et pH
. Pour un acide faible : Le pH est supérieur à celui d'un acide fort de même concentration ($pH > -\log C$).
. Pour une base faible : Le pH est inférieur à celui d'une base forte de même concentration.
4. La Constante d'Acidité ($K_A$ et $pK_A$)
La force d'un couple est caractérisée par sa constante à l'équilibre :
$K_A = \frac{[A^-]_{éq} \cdot [H_3O^+]_{éq}}{[AH]_{éq}}$
$pK_A = -\log K_A$
. Règle de classification : Un acide est d'autant plus fort que son $K_A$ est grand ou que son $pK_A$ est petit.
Que vous soyez élève au Lycée Moderne de Bangolo ou ailleurs, ce test vous permet de réviser des notions clés comme le coefficient d'ionisation ($\alpha$), l'équilibre chimique et l'effet de la dilution sur l'ionisation des espèces. Évaluez votre capacité à calculer les concentrations molaires des espèces chimiques présentes dans une solution faible et à interpréter les différences de pH entre solutions de même concentration. Un outil pédagogique essentiel pour réussir votre Baccalauréat ivoirien et maîtriser la chimie générale avec Kwiizoo.
1. Définitions Fondamentales
. Acide Faible : Espèce chimique dont la réaction avec l’eau est partielle (ou limitée).
Équation : $AH + H_2O \rightleftharpoons A^- + H_3O^+$
Exemple : L’acide éthanoïque ($CH_3COOH$).
. Base Faible : Espèce dont la réaction avec l’eau est incomplète.
Équation : $B + H_2O \rightleftharpoons BH^+ + OH^-$
Exemple : L’ammoniac ($NH_3$).
2. Le Coefficient d'Ionisation ($\alpha$)
C'est un élément clé de la page 29 du programme ivoirien.
. Formule : $\alpha = \frac{\text{quantité d'acide réagi}}{\text{quantité d'acide initial}}$
. Propriété : Pour un acide faible, $0 < \alpha < 1$. Plus la solution est diluée, plus $\alpha$ augmente (loi de dilution d'Ostwald).
3. Étude Quantitative et pH
. Pour un acide faible : Le pH est supérieur à celui d'un acide fort de même concentration ($pH > -\log C$).
. Pour une base faible : Le pH est inférieur à celui d'une base forte de même concentration.
4. La Constante d'Acidité ($K_A$ et $pK_A$)
La force d'un couple est caractérisée par sa constante à l'équilibre :
$K_A = \frac{[A^-]_{éq} \cdot [H_3O^+]_{éq}}{[AH]_{éq}}$
$pK_A = -\log K_A$
. Règle de classification : Un acide est d'autant plus fort que son $K_A$ est grand ou que son $pK_A$ est petit.
1 essai(s) il y a 1 jour(s)
10
AvancéSciences
0.0
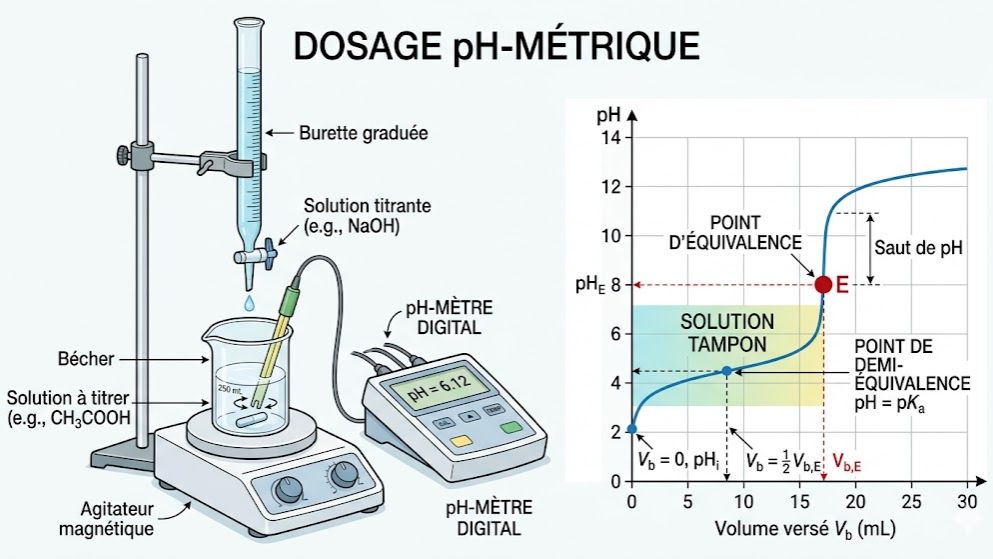
Maîtrisez les dosages et les solutions tampons avec ce quiz complet conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Ce test évalue votre compréhension des réactions entre acides et bases (forts et faibles), le tracé et l'exploitation des courbes pH-métriques, ainsi que la définition de l'équivalence.
Que vous soyez élève au Lycée Moderne d’Agboville ou ailleurs, révisez les caractéristiques essentielles des solutions tampons : leur préparation, leurs propriétés de résistance aux variations de pH et leur intérêt biologique ou agronomique. Apprenez à déterminer la demi-équivalence et la relation pH = pKa. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre comment stabiliser le pH dans des systèmes complexes avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
Réactions acido-basiques : Ce sont des transferts de protons $H^+$ entre un acide et une base. Elles sont généralement exothermiques et totales lorsqu'au moins l'un des réactifs est fort.
Dosage pH-métrique : Permet de déterminer la concentration d'une solution.
- Équivalence : Point où les réactifs ont été mélangés dans des proportions stoechiométriques.
- Demi-équivalence : Pour un dosage acide faible/base forte, à ce point, $pH = pK_A$.
Solution Tampon : Solution dont le pH varie très peu lors de l'ajout modéré d'un acide, d'une base ou lors d'une dilution.
- Préparation : Mélange équimolaire d'un acide faible et de sa base conjuguée, ou par demi-équivalence d'un dosage.
Que vous soyez élève au Lycée Moderne d’Agboville ou ailleurs, révisez les caractéristiques essentielles des solutions tampons : leur préparation, leurs propriétés de résistance aux variations de pH et leur intérêt biologique ou agronomique. Apprenez à déterminer la demi-équivalence et la relation pH = pKa. Un outil pédagogique indispensable pour exceller au Baccalauréat et comprendre comment stabiliser le pH dans des systèmes complexes avec Kwiizoo.
## Résumé du Cours (Aide-mémoire) ##
Réactions acido-basiques : Ce sont des transferts de protons $H^+$ entre un acide et une base. Elles sont généralement exothermiques et totales lorsqu'au moins l'un des réactifs est fort.
Dosage pH-métrique : Permet de déterminer la concentration d'une solution.
- Équivalence : Point où les réactifs ont été mélangés dans des proportions stoechiométriques.
- Demi-équivalence : Pour un dosage acide faible/base forte, à ce point, $pH = pK_A$.
Solution Tampon : Solution dont le pH varie très peu lors de l'ajout modéré d'un acide, d'une base ou lors d'une dilution.
- Préparation : Mélange équimolaire d'un acide faible et de sa base conjuguée, ou par demi-équivalence d'un dosage.
1 essai(s) il y a 6 heure(s)
10
AvancéSciences
0.0
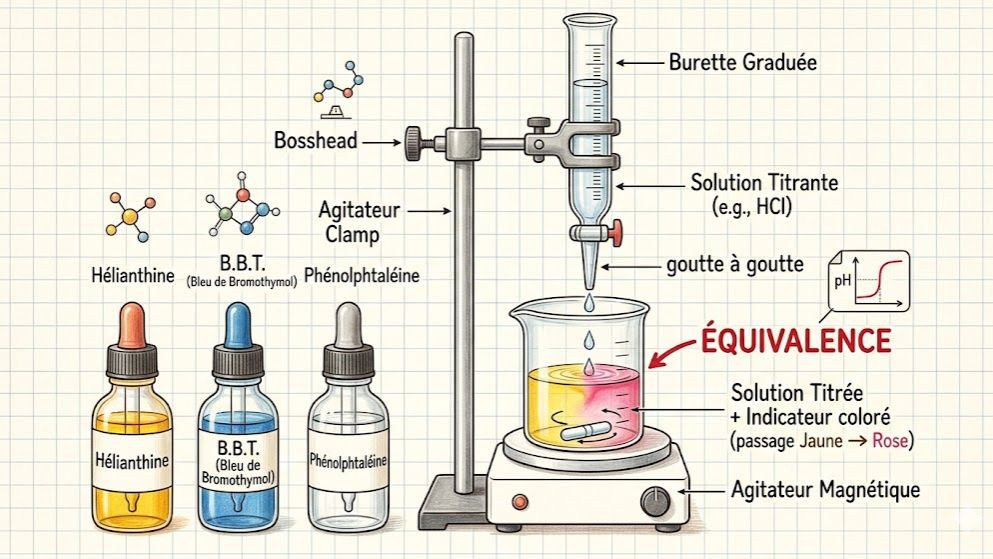
Maîtrisez les techniques de laboratoire avec ce quiz final sur le dosage acido-basique, conforme au programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. Testez votre capacité à déterminer la concentration d'une solution commerciale, comme le vinaigre, à travers le dosage colorimétrique. Que vous soyez élève au Lycée des Jeunes Filles de Bouaké ou ailleurs, ce test vous permet de réviser le protocole expérimental, le choix judicieux de l'indicateur coloré (B.B.T, hélianthine, phénolphtaléine) et le calcul des concentrations molaires à l'équivalence. Apprenez à schématiser un dispositif de dosage et à interpréter le changement de couleur pour identifier le point final.
Évaluez vos compétences sur la relation $C_A \cdot V_A = C_B \cdot V_B$ et comprenez l'intérêt industriel et domestique de ces mesures de précision. Un outil de révision ultime pour valider vos acquis avant le Baccalauréat avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Principe du dosage : Déterminer la concentration inconnue d'une espèce en solution en la faisant réagir totalement avec une autre espèce de concentration connue (le réactif titrant).
Dispositif expérimental : Comprend une burette graduée (contenant le réactif titrant), un bécher (contenant la solution à doser) et un agitateur magnétique.
Équivalence acido-basique : Moment où les réactifs ont été introduits dans des proportions stœchiométriques ; il y a changement de nature du milieu (de l'acide vers le basique ou inversement).
Dosage colorimétrique : Utilise un indicateur coloré dont la zone de virage contient le pH à l'équivalence pour visualiser le point final.
Application : Dosage de l'acide éthanoïque du vinaigre par une solution de soude.
Évaluez vos compétences sur la relation $C_A \cdot V_A = C_B \cdot V_B$ et comprenez l'intérêt industriel et domestique de ces mesures de précision. Un outil de révision ultime pour valider vos acquis avant le Baccalauréat avec Kwiizoo.
## Résumé du Cours (Aide-mémoire)
Principe du dosage : Déterminer la concentration inconnue d'une espèce en solution en la faisant réagir totalement avec une autre espèce de concentration connue (le réactif titrant).
Dispositif expérimental : Comprend une burette graduée (contenant le réactif titrant), un bécher (contenant la solution à doser) et un agitateur magnétique.
Équivalence acido-basique : Moment où les réactifs ont été introduits dans des proportions stœchiométriques ; il y a changement de nature du milieu (de l'acide vers le basique ou inversement).
Dosage colorimétrique : Utilise un indicateur coloré dont la zone de virage contient le pH à l'équivalence pour visualiser le point final.
Application : Dosage de l'acide éthanoïque du vinaigre par une solution de soude.
1 essai(s) il y a 5 heure(s)
10
AvancéSciences
0.0
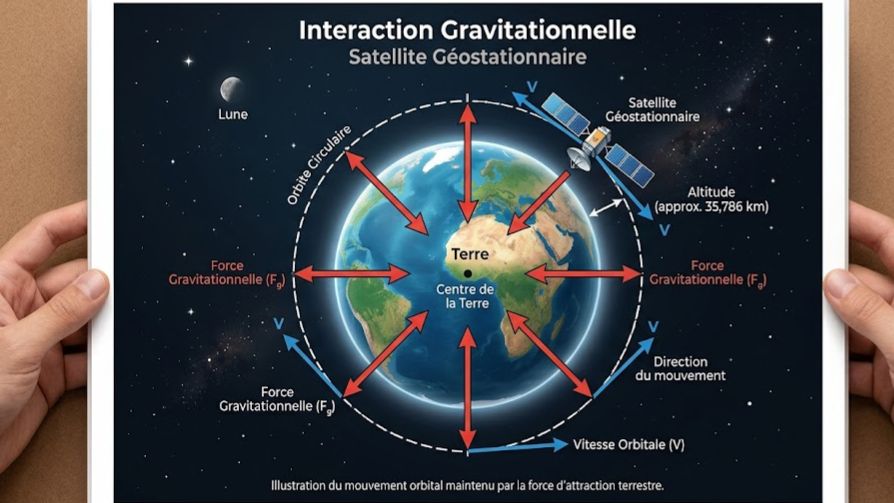
Maîtrisez les lois fondamentales de l'univers avec ce quiz complet sur l'interaction gravitationnelle, conçu spécifiquement selon le programme éducatif de Physique-Chimie de la Terminale C et D en Côte d'Ivoire. Que vous soyez élève au Lycée Moderne de Bingerville ou de Dimbokro, ce test vous permettra de réviser la loi d'attraction universelle de Newton, de comprendre le mouvement des satellites artificiels et de maîtriser la troisième loi de Kepler. Ce contenu pédagogique aborde les concepts clés tels que le champ gravitationnel à une altitude z, les caractéristiques d'un satellite géostationnaire (orbite circulaire dans le plan équatorial), et la notion d'impesanteur.
Testez vos connaissances sur le vecteur champ de pesanteur, le calcul de la masse d'une planète et la différence entre apogée et périgée. Un entraînement idéal pour réussir votre Baccalauréat et exceller dans le domaine des sciences physiques. Prêt à devenir un expert en mécanique céleste ? Lancez le quiz Kwiizoo maintenant !
Résumé du Cours (Aide-mémoire)
- Loi de Newton : Deux corps de masses $m_A$ et $m_B$ séparés par une distance $d$ s'attirent avec une force $F = G \cdot \frac{m_A \cdot m_B}{d^2}$.
- Champ de gravitation : À une altitude $h$ de la Terre, la valeur du champ est $g = G \cdot \frac{M_T}{(R_T + h)^2}$.
- Satellite géostationnaire : Il paraît immobile au-dessus d'un point de l'équateur. Ses caractéristiques sont : sa trajectoire est un cercle dans le plan équatorial, il tourne dans le même sens que la Terre, et sa période est égale à la période de rotation propre de la Terre (environ 24h).
- Lois de Kepler : La troisième loi (loi des périodes) stipule que pour toutes les planètes, le rapport $\frac{T^2}{r^3}$ est constant.
Testez vos connaissances sur le vecteur champ de pesanteur, le calcul de la masse d'une planète et la différence entre apogée et périgée. Un entraînement idéal pour réussir votre Baccalauréat et exceller dans le domaine des sciences physiques. Prêt à devenir un expert en mécanique céleste ? Lancez le quiz Kwiizoo maintenant !
Résumé du Cours (Aide-mémoire)
- Loi de Newton : Deux corps de masses $m_A$ et $m_B$ séparés par une distance $d$ s'attirent avec une force $F = G \cdot \frac{m_A \cdot m_B}{d^2}$.
- Champ de gravitation : À une altitude $h$ de la Terre, la valeur du champ est $g = G \cdot \frac{M_T}{(R_T + h)^2}$.
- Satellite géostationnaire : Il paraît immobile au-dessus d'un point de l'équateur. Ses caractéristiques sont : sa trajectoire est un cercle dans le plan équatorial, il tourne dans le même sens que la Terre, et sa période est égale à la période de rotation propre de la Terre (environ 24h).
- Lois de Kepler : La troisième loi (loi des périodes) stipule que pour toutes les planètes, le rapport $\frac{T^2}{r^3}$ est constant.
2 essai(s) il y a 6 jour(s)
10
AvancéSciences
0.0
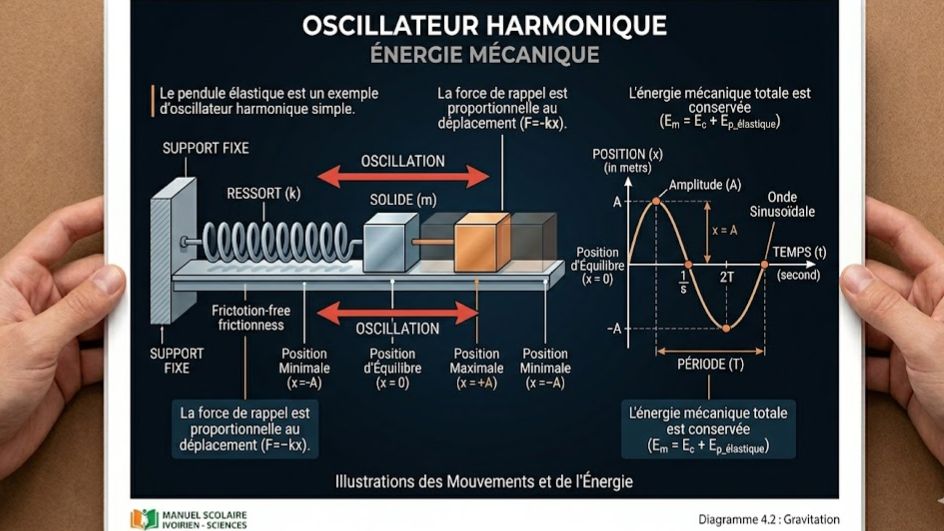
Maîtrisez le comportement des systèmes oscillants avec ce quiz sur les oscillations mécaniques libres, conçu selon le programme de Physique-Chimie de Terminale C et D en Côte d'Ivoire. À travers l'étude du pendule élastique et de l'oscillateur harmonique, ce test évalue votre compréhension des équations différentielles, de la conservation de l'énergie mécanique et des caractéristiques propres du mouvement comme la période, la pulsation et la fréquence.
Que vous soyez élève au Lycée Moderne Cocody-Angré ou ailleurs, ce contenu vous aide à différencier un oscillateur non amorti d'un système soumis à des frottements. Apprenez à exploiter les graphes $x(t)$ et $v(t)$ et comprenez le rôle crucial des amortisseurs dans la sécurité routière. Préparez votre Baccalauréat avec Kwiizoo, l'application de référence pour l'excellence académique en Côte d'Ivoire.
Résumé du Cours (Aide-mémoire)
Définition : Un oscillateur mécanique est un système qui effectue un mouvement de va-et-vient de part et d'autre de sa position d'équilibre stable.
Équation Différentielle : Pour un ressort de constante de raideur $k$ et une masse $m$ (sans frottement), l'équation s'écrit : $\ddot{x} + \frac{k}{m}x = 0$.
Solution : La solution est de forme sinusoïdale : $x(t) = X_m \cos(\omega_0t + \phi)$.
Caractéristiques :
Pulsation propre : $\omega_0 = \sqrt{\frac{k}{m}}$.
Période propre : $T_0 = 2\pi\sqrt{\frac{m}{k}}$.
Énergie : Dans un oscillateur harmonique non amorti, l'énergie mécanique $E_m$ se conserve ($E_m = E_c + E_{pe} = \text{constante}$).
Que vous soyez élève au Lycée Moderne Cocody-Angré ou ailleurs, ce contenu vous aide à différencier un oscillateur non amorti d'un système soumis à des frottements. Apprenez à exploiter les graphes $x(t)$ et $v(t)$ et comprenez le rôle crucial des amortisseurs dans la sécurité routière. Préparez votre Baccalauréat avec Kwiizoo, l'application de référence pour l'excellence académique en Côte d'Ivoire.
Résumé du Cours (Aide-mémoire)
Définition : Un oscillateur mécanique est un système qui effectue un mouvement de va-et-vient de part et d'autre de sa position d'équilibre stable.
Équation Différentielle : Pour un ressort de constante de raideur $k$ et une masse $m$ (sans frottement), l'équation s'écrit : $\ddot{x} + \frac{k}{m}x = 0$.
Solution : La solution est de forme sinusoïdale : $x(t) = X_m \cos(\omega_0t + \phi)$.
Caractéristiques :
Pulsation propre : $\omega_0 = \sqrt{\frac{k}{m}}$.
Période propre : $T_0 = 2\pi\sqrt{\frac{m}{k}}$.
Énergie : Dans un oscillateur harmonique non amorti, l'énergie mécanique $E_m$ se conserve ($E_m = E_c + E_{pe} = \text{constante}$).
2 essai(s) il y a 6 jour(s)
10
Commentaires (0)
Connectez-vous pour commenter
Cliquez ici pour vous connecter